Cho 3 pin Galvani đơn giản được thiết lập như sau:
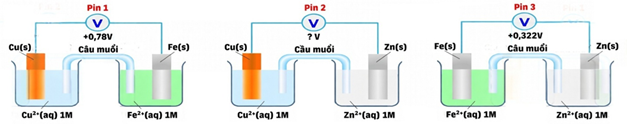
Cho nguyên tử khối: Zn = 65,38 amu; Cu = 63,546 amu và Fe = 55,845 amu.
a) Giá trị sức điện động của pin 2 bằng +1,12 V.
b) Sau 3 pin ngừng hoạt động, nhấc hai điện cực ra cân lại thấy tổng khối lượng của hai điện cực của cả 3 pin đều tăng so với ban đầu.
c) Khi làm điện cực, kẽm luôn đóng vai trò là anode, đồng luôn đóng vai trò là cathode.
d) Thứ tự chuẩn của các cặp oxi hóa – khử liên quan đến ba pin trên có giá trị giảm dần như sau: Cu2+/Cu > Fe2+/Fe > Zn2+/Zn.
Câu trả lời tốt nhất
(a) Sai, E°Zn-Cu = E°Zn-Fe + E°Fe-Cu = 0,322 + 0,78 = 1,102V
(b) Sai, phản ứng trong 3 pin:
(1) Fe + Cu2+ —> Fe2+ + Cu
(2) Zn + Cu2+ —> Zn2+ + Cu
(3) Zn + Fe2+ —> Zn2+ + Fe
Chỉ pin (1) có tổng khối lượng điện cực tăng (55,845 < 63,546). Pin (2)(3) có tổng khối lượng điện cực giảm (do nguyên tử khối của Zn lớn hơn Fe, Cu).
(c) Đúng, tính khử Zn > Fe > Cu nên Zn luôn là anode, Cu luôn là cathode trong 3 pin trên.
(d) Đúng, tính khử của dạng khử càng mạnh, thế điện cực chuẩn càng âm nên Cu2+/Cu > Fe2+/Fe > Zn2+/Zn.

