Cho bột nhôm tan hoàn toàn vào dung dịch H2SO4, thu được 6,72 lít khí H2 (đktc) và dung dịch X. Cho từ từ dung dịch Ba(OH)2 1M đến dư vào X. Đồ thị biểu diễn sự phụ thuộc giữa khối lượng kết tủa (y, gam) vào thể tích dung dịch Ba(OH)2 1M (V, lit) như sau:
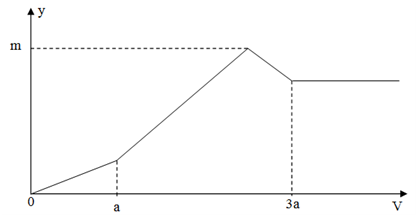
Giá trị của m là
A. 136,2. B. 147,7. C. 132,1. D. 155,4.
Câu trả lời tốt nhất
nH2 = 0,3 —> nAl3+ = 0,2
Đoạn 1:
OH- + H+ —> H2O
Ba2+ + SO42- —> BaSO4
—> nH+ = nOH- đoạn này = 2a
Khi kết tủa không thay đổi thì: nBa(OH)2 đã dùng = 3a; nBa(AlO2)2 = 0,1 —> nBaSO4 = 3a – 0,1
Dung dịch X chứa Al3+ (0,2), H+ (2a), SO42- (3a – 0,1)
Bảo toàn điện tích —> a = 0,2
Đoạn 2:
Ba2+ + SO42- —> BaSO4
3OH- + Al3+ —> Al(OH)3
—> nBaSO4 = nSO42- = 0,5 và nAl(OH)3 = nAl3+ = 0,2
—> m↓ = 132,1 gam
×

