Dinitrogen tetroxide (không màu) bị phân huỷ thành nitrogen dioxide (màu nâu đỏ) theo phản ứng: N2O4(g) ⇋ 2NO2(g)
Ban đầu, trong bình phản ứng dung tích không đổi 1 Lít có chứa 0,6 mol N2O4. Thời gian đạt tới trạng thái cân bằng và nồng độ N2O4 ở các nhiệt độ khác nhau như sau:
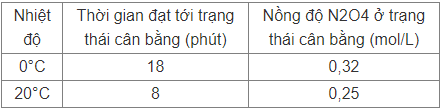
a) Khi tăng nhiệt độ, màu sắc hỗn hợp khí trong bình thay đổi như thế nào? Giải thích?
b) Tính hằng số cân bằng Kc của phản ứng trên ở 20°C.
Câu trả lời tốt nhất
(a) Khi tăng nhiệt độ, nồng độ N2O4 giảm nên nồng độ NO2 tăng —> Màu sắc hỗn hợp đậm dần.
(b) Ở 20°C: [N2O4] = 0,25 mol/L
—> [NO2] = 2(0,6 – 0,25) = 0,7 mol/L
—> Kc = [NO2]²/[N2O4] = 1,96
×

