Hợp chất X được sử dụng làm thuốc pháo, ngòi nổ, thuốc đầu diêm, thuốc giúp cây nhãn ra hoa… X có khối lượng mol bằng 122,5 g/mol, chứa ba nguyên tố A, Y, E. Trong phân tử X có 1 nguyên tử A, 1 nguyên tử Y. Thành phần phần trăm khối lượng nguyên tố E trong X bằng 39,19%. Nguyên tố E có 4 electron p.
a) Xác định công thức phân tử của X?
b) Viết công thức Lewis và chỉ rõ các loại liên kết hóa học có trong phân tử X?
Câu trả lời tốt nhất
(a)
Nguyên tố E có 4 electron p (1s2 2s2 2p4) nên E là O
Số nguyên tử O trong X = 122,5.39,19%/16 = 3
MX = A + Y + 16.3 = 122,5
—> A + Y = 74,5
Chọn A = 39 (K) và Y = 35,5 (Cl) (Có thể tráo đổi A và Y)
CTPT của X là KClO3.
(b) Công thức Lewis của KClO3:
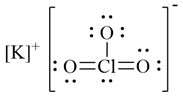
Các loại liên kết hóa học có trong phân tử KClO3:
+ Liên kết ion giữa K+ và ClO3-.
+ Liên kết cộng hóa trị giữa Cl và O.

