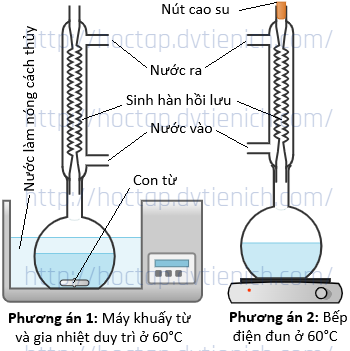
Một nhóm học sinh tiến hành thí nghiệm điều chế nitrobenzene theo phương án 1 như hình vẽ. Cho con từ vào bình cầu, thêm 30 mL H2SO4 đặc, làm lạnh trong chậu nước đá rồi thêm từ từ 30 mL HNO3 đặc, sau đó cho 10 mL benzene và lắp sinh hàn hồi lưu rồi đun cách thủy trong 60 phút. Biết rằng, máy khuấy từ cung cấp nhiệt lượng đồng thời hệ thống nam châm quay tạo từ trường làm xoay con từ bên trong bình cầu.
a) Viết phương trình hóa học của phản ứng và nêu hiện tượng quan sát được trong bình cầu khi ngừng khuấy, để yên hỗn hợp (khối lượng riêng của nitrobenzene là 1,2 g/cm³).
b) Sau phản ứng nitro hóa, hỗn hợp chất lỏng trong bình cầu gồm: nitrobenzene, benzene dư, các acid và nước. Biết CaCl2 khan có khả năng hút ẩm, nhiệt độ sôi của benzene là 80,1°C và của nitrobenzene là 210,9°C. Hãy trình bày các bước (sử dụng kỹ thuật chiết và chưng cất) tách loại tạp chất để thu được nitrobenzene.
c) Theo quy định an toàn, thí nghiệm này bắt buộc phải tiến hành trong tủ hút. Xác định các khí hoặc hơi độc hại thoát ra từ đầu ống sinh hàn hồi lưu trong quá trình đun nóng và giải thích nguồn gốc sinh ra chúng.
d) Một học sinh đề xuất tiến hành thí nghiệm theo phương án 2 như hình vẽ vì cho rằng:
– Không cần con từ khuấy hỗn hợp cho nên thay máy khuấy từ bằng bếp điện.
– Để ngăn khí độc thoát ra ngoài thì đậy kín đầu trên của ống sinh hàn hồi lưu.
Hãy đánh giá tính khả thi và dự báo những rủi ro có thể xảy ra khi tiến hành theo phương án này. Giải thích.
Câu trả lời tốt nhất
(a) Phản ứng:
C6H6 + HNO3 đặc (H2SO4 đặc, 60°C) —> C6H5NO2 + H2O
Khi ngừng khuấy hỗn hợp trong bình cầu phân lớp: lớp chất lỏng như dầu, màu vàng nhạt nổi lên trên là C6H5NO2 có lẫn benzene dư. Lớp chất lỏng phía dưới là các dung dịch acid đặc H2SO4, HNO3.
(b) Dùng phương pháp chiết:
+ Cho toàn bộ chất lỏng trong bình cầu vào phễu chiết.
+ Xả bỏ phần chất lỏng phía dưới, thu lấy phần chất lỏng phía trên (C6H5NO2/C6H6) vào cốc thủy tinh.
+ Thêm CaCl2 khan vào cốc để làm khô hỗn hợp C6H5NO2/C6H6.
Dùng phương pháp chưng cất:
+ Lọc bỏ CaCl2, cho chất lỏng còn lại vào bình chưng cất có ống sinh hàn. Dùng nhiệt kế để kiểm soát nhiệt độ.
+ Tiến hành chưng cất ở 80,1°C, benzene sôi, bay lên và ngưng tụ trong ống sinh hàn, được hứng vào cốc khác.
+ Khi nhiệt độ bắt đầu tăng là lúc benzene đã bay ra hết. Dừng chưng cất, chất lỏng còn lại trong bình là C6H5NO2.
(c) Các hơi thoát ra ở đầu ống sinh hàn:
+ C6H6: chất này là nguyên liệu ban đầu, dễ bay hơi, độc hại.
+ NO2: khí độc, sinh ra do HNO3 bị phân hủy bởi nhiệt độ (4HNO3 —> 4NO2 + O2 + 2H2O)
+ HNO3: hơi ăn mòn mạnh, nguồn gốc từ nguyên liệu ban đầu.
(d) Nếu không dùng con từ:
+ Hỗn hợp không được trộn đều, benzene dễ tách lớp do không tan và nhẹ hơn.
+ Tại vị trí phân lớp phản ứng nitro hóa có thể xảy ra mất kiểm soát (do đây là phản ứng tỏa nhiệt), có thể thế các vị trí khác trên vòng benzene.
Nếu dùng bếp điện: Khó điều chỉnh nhiệt độ cho phù hợp, phần tiếp giáp giữa bình cầu và bếp sẽ có nhiệt độ quá cao.
Nếu bịt kín đầu trên của ống sinh hàn: Ống sinh hàn không thể hóa lỏng toàn bộ các chất hơi bay lên khiến áp suất tăng rất nhanh, các khớp nối có thể bị bật ra hoặc nổ bình. Các hóa chất độc hại và ăn mòn mạnh bắn ra gây nguy hiểm.

