Một pin Galvani được thiết lập ở điều kiện chuẩn theo sơ đồ sau:
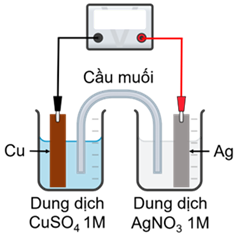
Câu 1. Cho E°Cu2+/Cu = 0,34V; E°Ag+/Ag = 0,799V.
a) Thanh Cu là cực âm (anode), tại đây xảy ra quá trình oxi hóa.
b) Khi pin hoạt động, electron di chuyển từ thanh Cu sang thanh Ag.
c) Nếu thay thanh Ag ngâm trong dung dịch AgNO3 1M bằng thanh Zn ngâm trong dung dịch Zn(NO3)2 1M thì tại thanh Cu xảy ra quá trình khử.
d) Sau khi pin hoạt động 1 thời gian, lấy thanh Ag làm sạch rồi nhúng vào cốc chứa dung dịch CuSO4 sẽ xảy ra hiện tượng ăn mòn điện hóa.
Câu 2. Cầu muối chứa muối NH4NO3. Khi pin Galvani trên hoạt động:
a) Phản ứng xảy ra trong pin Galvani trên là: Cu(s) + Ag+(aq) → Cu+(aq) + Ag(s).
b) Phản ứng hóa học diễn ra trong pin Galvani trên giải phóng năng lượng.
c) Có dòng electron di chuyển qua dây dẫn điện từ điện cực Cu sang điện cực Ag.
d) Ion NH4+ trong cầu muối di chuyển về dung dịch bên anode, còn ion NO3- di chuyển về dung dịch bên cathode.
Câu trả lời tốt nhất
Câu 1.
(a) Đúng, anode là thanh Cu, tại đây xảy ra quá trình oxi hóa Cu:
Cu —> Cu2+ + 2e
(b) Đúng, khi pin hoạt động, electron di chuyển từ thanh Cu qua dây dẫn sang thanh Ag.
(c) Đúng, nếu thay Ag/AgNO3 bằng Zn/Zn(NO3)2 thì thanh Cu lại thành cathode, tại đây sẽ xảy ra sự khử Cu2+.
(d) Sai, Ag không khử được Cu2+ nên nhúng thanh Ag vào dung dịch CuSO4 sẽ không có ăn mòn điện hóa.
Câu 2.
(a) Sai, phản ứng xảy ra trong pin Galvani trên là: Cu(s) + 2Ag+(aq) → Cu2+(aq) + 2Ag(s).
(b) Đúng, năng lượng từ phản ứng hóa học trên đã chuyển hóa thành điện năng giúp pin hoạt động.
(c) Đúng, khi pin hoạt động electron từ điện cực Cu di chuyển qua dân dẫn đến điện cực Ag.
(d) Sai, Cu là anode, tại đây Cu bị oxi hóa thành Cu2+ nên ion NO3- sẽ di chuyển tới để trung hòa điện tích của Cu2+. Ag là cathode, tạid dây Ag+ bị khử thành Ag nên NH4+ sẽ di chuyển tới để trung hòa điện tích của NO3-.

