Năng lượng liên kết và nhiệt độ sôi của các hydrogen halide như bảng sau:
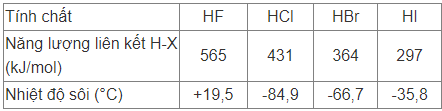
a) Nêu và giải thích quy luật biến đổi năng lượng liên kết H-X trong dãy: HF, HCl, HBr, HI.
b) Giải thích quy luật biến đổi nhiệt độ sôi của HCl, HBr, HI và giải thích sự bất thường về nhiệt độ sôi của HF so với các hydrogen halide còn lại.
Câu trả lời tốt nhất
(a) Năng lượng liên kết H-X giảm dần trong dãy: HF, HCl, HBr, HI vì bán kính các anion F-, Cl-, Br-, I- tăng dần làm độ dài liên kết tăng dần và mật độ điện tích âm trên các anion giảm dần —> Lực liên kết giảm dần.
(b) Nhiệt độ sôi của HCl, HBr, HI tăng dần do khối lượng phân tử tăng dần.
HF có nhiệt độ sôi cao hơn hẳn các HX còn lại vì giữa các phân tử HF có liên kết H liên phân tử, các HX còn lại không có liên kết H liên phân tử.

