Ở 20°C, hòa tan hết hỗn hợp chất rắn X gồm CuSO4 và FeCl3 (nCuSO4 > nFeCl3) vào 140 gam nước. Điện phân dung dịch thu được bằng dòng điện một chiều có cường độ không đổi, sự thay đổi của khối lượng dung dịch (gam) theo thời gian điện phân (giây) được biểu diễn bằng đồ thị sau:
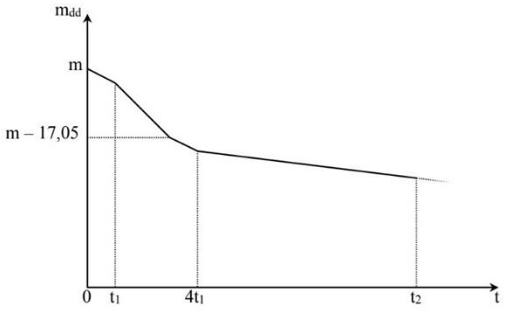
Biết t2 = 12t1. Nồng độ phần trăm của muối có trong dung dịch tại thời điểm t2 là
A. 8%. B. 10%. C. 12%. D. 14%.
Câu trả lời tốt nhất
nFeCl3 = a và nCuSO4 = b. Đặt c = It1/F
Đoạn 1:
2FeCl3 —> 2FeCl2 + Cl2
a………………..a………0,5a
—> ne = a = c (1)
Đoạn 2:
CuSO4 + FeCl2 —> Cu + Cl2 + FeSO4
a…………….a………..a…….a
—> m giảm = 64a + 71(a + 0,5a) = 17,05
—> a = 0,1 (2)
Đoạn 3:
CuSO4 + H2O —> Cu + 0,5O2 + H2SO4
b-0,1……………….b-0,1….0,5(b-0,1)
ne = 2(a + 0,5a) + 4.0,5(b – 0,1) = 4c (3)
(1)(2)(3) —> a = c = 0,1 và b = 0,15
Đoạn 4 trở đi chỉ còn điện phân H2O, trong đoạn này ne = 8c = 0,8, ứng với 0,4 mol H2O đã bị điện phân.
m giảm = 17,05 + 80(b – 0,1) + 0,4.18 = 28,25
mdd = mX + mH2O – m giảm = 152
nFeSO4 = a —> C%FeSO4 = 10%
Ad ơi giải thik hộ e cái đoạn 4 thấy chỗ 3c sao sao á nó phải bằng 8c chứ @@

