Tiến hành điện phân dung dịch chứa m gam hỗn hợp CuSO4 và KCl bằng dòng điện một chiều có cường độ 2A (điện cực trơ, có màng ngăn xốp). Kết quả thí nghiệm được ghi trong bảng sau:
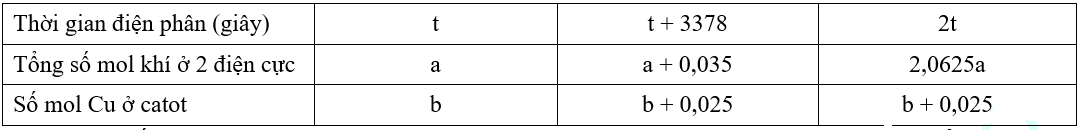
Giả sử hiệu suất điện phân 100%, các khí sinh ra không tan trong dung dịch. Giá trị của m gần nhất với:
A. 17,00 B. 14,7 C. 18,6 D. 16,00
Câu trả lời tốt nhất
Lượng electron trao đổi trong khoảng thời gian 3378 giây là 3378.2/96500 = 0,07 mol.
Trong khoảng thời gian này thì:
+ Catot thoát ra 0,025 mol Cu, dễ thấy 0,025.2 < 0,07 nên phải có thêm H2 thoát ra. Vậy nH2 = (0,07 – 0,025.2)/2 = 0,01
+ Hai điện cực thoát ra 0,035 mol khí, trong đó có H2 (0,01) và khí còn lại 0,035 – 0,01 = 0,025 mol. Vì ne = 0,07 nên khí còn lại này gồm Cl2 (0,015) và O2 (0,01)
Thời điểm t giây chưa thoát H2 và O2 nên a = b (1)
Thời điểm 2t giây: ne = 4a = 4b
+ Catot: ne = 2nCu + 2nH2 —> nH2 = b – 0,025
+ Tổng khí = nCl2 + nH2 + nO2 = (a + 0,015) + (b – 0,025) + [4a – 2(a + 0,015)]/4 = 2,0625a (2)
(1)(2) —> a = b = 0,04
nCuSO4 = b + 0,025 = 0,065
nKCl = 2(a + 0,015) = 0,11
—> m = 18,595

