Trong công nghiệp, aluminium (nhôm) được sản xuất từ quặng bauxite theo hai giai đoạn chính:
Giai đoạn 1: Tinh chế quặng bauxite.
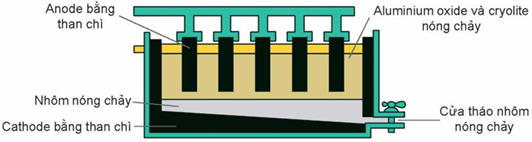
Giai đoạn 2: Điện phân Al2O3 nóng chảy. Sơ đồ thùng điện phân Al2O3 nóng chảy:
Câu 1.
a) Trung bình để sản xuất được 5,4 tấn Al thì lượng điện cực than chì bị tiêu hao do phản ứng oxi hoá là 2 tấn. (Giả thiết thành phần khí bay ra ở cực dương gồm 20% CO và 80% CO2 về thể tích).
b) Cryolite được thêm vào bể điện phân giúp tiết kiệm được năng lượng, giảm chi phí sản xuất.
c) Aluminium oxide được hòa tan trong cryolite nóng chảy và Al được thu lấy ở cực dương.
d) Cực dương bị mòn dần theo thời gian và cần được thay thế thường xuyên.
Câu 2.
a. Vì anode và cathode đều làm bằng graphite, nên nếu đổi chiều dòng điện (anode trở thành cathode và ngược lại) thì quy trình điện phân vẫn xảy ra bình thường.
b. Alumium oxide được hòa tan trong cryolite nóng chảy và Al được thu lấy ở cực dương.
c. Một loại quặng bauxite chứa khoảng 48% Al2O3 còn lại là các tạp chất khác. Giả thiết trong quá trình sản xuất chỉ có 95% lượng nhôm trong quặng chuyển hóa thành kim loại. Để sản xuất được 4 tấn nhôm thì khối lượng quặng bauxite cần dùng là 22,4 tấn.
d. Thành phần chính của quặng bauxite là Al2O3.2H2O.
Câu trả lời tốt nhất
Câu 1.
(a) Đúng:
nAl = 0,2; nCO = x; nCO2 = 4x (đơn vị đều là triệu mol)
Bảo toàn electron: 0,2.3 = 2x + 4.4x
—> x = 1/30 —> mC = 12.5x = 2 tấn
(b) Đúng, cryolite giúp giảm nhiệt độ nóng chảy, tăng độ dẫn điện, nhờ đó tiết kiệm được năng lượng, giảm chi phí sản xuất.
(c) Sai, Al thu được từ cực âm (cathode).
(d) Đúng, cực dương bị oxi hóa nên được hạ thấp dần đến khi hết thì phải thay mới.
Câu 2.
(a) Sai, nếu đổi điện cực thì cathode lại ở phía trên, Al lỏng vẫn sinh ra nhưng nặng hơn và chìm xuống và gặp các khí O2, CO, CO2 đang đi lên gây ra phản ứng tái tạo Al2O3. Điện cực anode phía dưới bị ăn mòn cũng khó thay thế.
(b) Sai, Al thu được từ cực âm (cathode).
(c) Sai
m quặng = 4.102/(2.27.48%.95%) = 16,6 tấn
(d) Đúng

