Trong công nghiệp, nhôm được điều chế bằng cách điện phân nóng chảy hỗn hợp alumina (Al2O3) và cryolite (Na3AlF6) còn gọi là quy trình Hall-Héroul: 2Al2O3(l) → 4Al(l) + 3O2(g) như hình dưới đây:
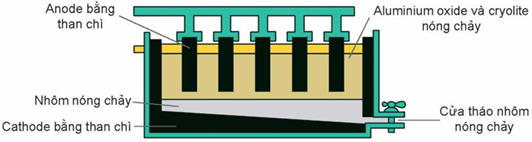
a) Nhôm kim loại được tách ra tại cathode.
b) Cryolite được thêm vào bể điện phân giúp tiết kiệm được năng lượng, giảm chi phí sản xuất.
c) Quy trình Hall-Héroult thu được nhôm tinh khiết và oxygen tinh khiết.
d) Trong quá trình điện phân, nếu đổi chiều dòng điện (anode trở thành cathode và ngược lại) thì quá trình điện phân vẫn xảy ra như trước khi đổi chiều dòng điện.
e) Cho biết phương trình nhiệt hóa học: 2Al2O3(s) → 4Al(s) + 3O2(g),  = 1676,00 kJ. Để thu được 1 tấn Al với hiệu suất sử dụng năng lượng đạt 75 % thì cần tiêu tốn 5747,6 kWh (1 kWh = 3,6.10^6 J).
= 1676,00 kJ. Để thu được 1 tấn Al với hiệu suất sử dụng năng lượng đạt 75 % thì cần tiêu tốn 5747,6 kWh (1 kWh = 3,6.10^6 J).
Câu trả lời tốt nhất
(a) Đúng
(b) Đúng, cryolite được thêm vào bể điện phân giúp giảm nhiệt độ nóng chảy của Al2O3, tăng độ dẫn điện, qua đó tiết kiệm được năng lượng, giảm chi phí sản xuất.
(c) Sai, tại anode O2 sinh ra đốt cháy điện cực nên sản phẩm khí gồm CO, CO2, O2.
(d) Sai, nếu đổi chiều dòng điện thì Al nóng chảy sinh ra nặng hơn nên rơi xuống, hỗn hợp khí CO, CO2, O2 đi lên, chúng gặp nhau sẽ xảy ra các tương tác hóa học và không thu được Al ở cửa thoát nữa.
(e) Đúng
mAl = 1 tấn và H = 75% nên năng lượng tiêu tốn là:
E = 10^6.1676/(27.4.75%) = 20691358 kJ = 5747,6 kWh

