Xét quá trình hoạt động của một pin điện hoá Cu-Ag được thiết lập ở các điều kiện như hình vẽ bên. Cho E°Cu2+/Cu = +0,340V và E°Ag+/Ag = +0,799 V.
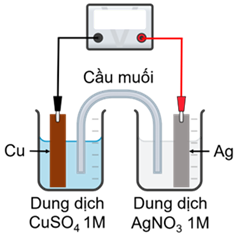
a. Viết phương trình của các quá trình xảy ra tại anode, cathode và phương trình hóa học của phản ứng xảy ra khi pin hoạt động.
b. Tính sức điện động chuẩn của pin.
c. Trong quá trình pin hoạt động khối lượng các điện cực Cu và Ag thay đổi như thế nào?
Câu trả lời tốt nhất
(a) Anode (Cu): Cu —> Cu2+ + 2e
Cathode (Ag): Ag+ + 1e —> Ag
Phản ứng: Cu + 2Ag+ —> Cu2+ + 2Ag
(b) E° = E°Ag+/Ag – E°Cu2+/Cu = 0,459V
(c) Trong quá trình pin hoạt động, khối lượng điện cực Cu giảm xuống vì Cu tan vào dung dịch và khối lượng điện cực Ag tăng lên vì có thêm Ag bám vào.
×

