Câu 1. Tiến hành điện phân 400 ml dung dịch chứa CuSO4 xM và NaCl yM bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi I = 5A. Quá trình điện phân được ghi nhận theo bảng sau:
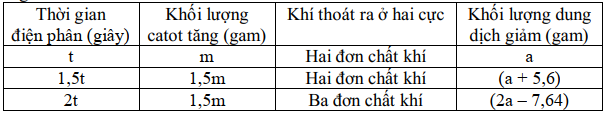
Cho các nhận định sau:
(a) Giá trị của m là 8,96 gam.
(b) Giá trị của a là 14,5 gam.
(c) Giá trị của t là 5404 giây.
(d) Tỉ lệ x : y là 3 : 2.
Biết các khí sinh ra không tan trong dung dịch và hiệu suất quá trình điện phân đạt 100%. Số nhận định đúng là
A. 2. B. 4. C. 1. D. 3.
Câu 2. Tiến hành điện phân 400 ml dung dịch chứa CuSO4 xM và NaCl yM với cường độ dòng điện không đổi bằng điện cực trơ, màng ngăn xốp. Quá trình điện phân được ghi nhận theo bảng sau:
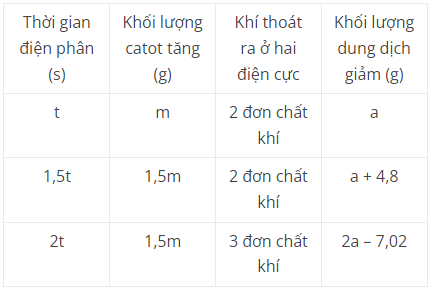
Biết các khi sinh ra không tan trong dung dịch và hiệu suất của quá trình điện phân đạt được 100%.
1) Tính x + y.
2) Khi thời gian 2,5t thì dừng điện phân, dung dịch thu được trong bình điện phân tại thời điểm này hòa tan tối đa bao nhiêu gam Al2O3?
Câu trả lời tốt nhất
Câu 1.
nCuSO4 = 0,4x; nNaCl = 0,4y
Trong khoảng thời gian 0,5t giây (tính từ t đến 1,5t), catot thoát ra 0,5m gam Cu —> Anot thoát nO2 = nCu/2 = m/256
—> m giảm = 0,5m + 32m/256 = 5,6
—> m = 8,96
—> nCuSO4 = 0,4x = 1,5m/64 —> x = 0,525
ne trong t giây = 2m/64 = 0,28 = It/F —> t = 5404
Tại thời điểm t giây:
Catot: nCu = 0,14
Anot: nCl2 = 0,2y, bảo toàn electron —> nO2 = 0,07 – 0,1y
m giảm = 8,96 + 71.0,2y + 32(0,07 – 0,1y) = a (1)
Tại thời điểm 2t giây (ne = 0,56)
Catot: nCu = 0,21; nH2 = 0,07
Anot: nCl2 = 0,2y, bảo toàn electron —> nO2 = 0,14 – 0,1y
m giảm = 0,21.64 + 0,07.2 + 71.0,2y + 32(0,14 – 0,1y) = 2a – 7,64 (2)
(1)(2) —> y = 0,3; a = 14,5
(a)(b)(c) Đúng
(d) Sai, x : y = 7 : 4
Câu 2.
nCuSO4 = 0,4x; nNaCl = 0,4y
Trong khoảng thời gian 0,5t giây (tính từ t đến 1,5t), catot thoát ra 0,5m gam Cu —> Anot thoát nO2 = nCu/2 = m/256
—> m giảm = 0,5m + 32m/256 = 4,8
—> m = 7,68
—> nCuSO4 = 0,4x = 1,5m/64 —> x = 0,45
ne trong t giây = 2m/64 = 0,24
Tại thời điểm t giây:
Catot: nCu = 0,12
Anot: nCl2 = 0,2y, bảo toàn electron —> nO2 = 0,06 – 0,1y
m giảm = 7,68 + 71.0,2y + 32(0,06 – 0,1y) = a (1)
Tại thời điểm 2t giây (ne = 0,48)
Catot: nCu = 0,18; nH2 = 0,06
Anot: nCl2 = 0,2y, bảo toàn electron —> nO2 = 0,12 – 0,1y
m giảm = 0,18.64 + 0,06.2 + 71.0,2y + 32(0,12 – 0,1y) = 2a – 7,02 (2)
(1)(2) —> y = 0,3; a = 12,9
—> x + y = 0,75
Thời điểm 2,5t giây, dung dịch sau điện phân chứa SO42- (0,18), Na+ (0,12), bảo toàn điện tích —> nH+ = 0,24
—> nAl2O3 = nH+/6 = 0,04 —> mAl2O3 = 4,08 gam

