Để tiến hành mạ một tấm huy chương hình trụ, đáy tròn với bán kính 2,5 cm; chiều cao hình trụ 0,3 cm; với lớp mạ bằng copper dày 0,1 cm như hình bên.
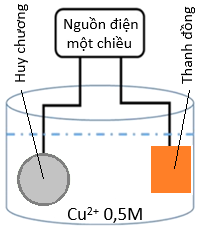
Người ta có thể tiến hành điện phân dung dịch X (CuSO4) nồng độ 0,5M, dư với cường độ dòng điện không đổi 2A, khi kết thúc điện phân (quá trình mạ hoàn thành) thì hết thời gian là t giây. Biết khối lượng riêng của copper là 8,95 g/cm³ và hiệu suất điện phân là 100%, giả thiết lớp mạ huy chương dày như nhau, toàn bộ lượng copper tạo ra đều bám hết vào tấm huy chương. Cho hằng số Faraday F = 96500, π = 3,14.
a) Thanh copper là cực dương, huy chương được mạ sẽ đóng vai trò cực âm.
b) Khi kết thúc điện phân bên điện cực anode thoát ra 8,193 lít (đkc).
c) Chiều dòng electron di chuyển từ huân chương được mạ qua dây dẫn đến thanh copper.
d) Thời gian điện phân 64800 giây.
Câu trả lời tốt nhất
(a) Đúng
(b) Sai, tại anode: Cu —> Cu2+ + 2e, không có khí O2 thoát ra.
(c) Sai, chiều dòng electron di chuyển từ thanh Cu, qua nguồn điện đến tấm huy chương. Nguồn điện đóng vai trò giống như “máy bơm” electron.
(d) Sai
Trước mạ: r = 2,5 cm; h = 0,3 cm —> V = 5,8875 cm³
Sau khi mạ: r = 2,5 + 0,1 = 2,6 cm; h = 0,3 + 0,1.2 = 0,5 cm —> V = 10,6132
(Công thức V = πr²h, trong đó π = 3,14)
—> mCu = 8,95(V sau – V trước) = 42,295015 gam
mCu = 64It/2F —> t = 63773s

