Một nhóm học sinh muốn sử dụng phương pháp điện phân để mạ đồng (copper) cho chiếc chìa khóa làm bằng thép (hợp kim Fe-C). Nhóm học sinh đã lấy một đồng xu bằng hợp kim Cu – Zn (trong đó Cu chiếm 95% về khối lượng). Chuẩn bị dung dịch điện phân là 300mL dung dịch copper (II) sulfate 0,5M.
Nhóm học sinh đưa ra giả thuyết: “Trong cùng một khoảng thời gian điện phân, nếu tăng cường độ dòng điện thì lượng đồng bám lên chìa khóa sẽ tăng”. Để kiểm chứng giả thuyết, nhóm học sinh tiến hành thực nghiệm như sau:
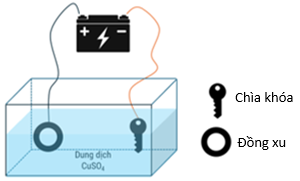
Sau mỗi khoảng thời gian điện phân x phút, lấy ra làm khô, rồi cân để xác định lại khối lượng của chìa khóa. Nhóm học sinh điều chỉnh cường độ dòng điện tăng thêm 0,5A rồi tiếp tục điện phân. Kết quả thực nghiệm được ghi lại trong bảng sau:
Thời điểm…. Ban đầu… x phút… 2x phút… 3x phút
Cường độ (A)………………… I……… I + 0,5……. I + 1
m chìa khoá…. 18,2………. 18,6……… 19,1……… m
(Giả sử toàn bộ đồng sinh ra bám hết lên chìa khoá, hiệu suất điện phân không thay đổi). Số mol electron mà nguyên tử hoặc ion đã cho hoặc nhận được tính theo công thức Trong đó, I là cường độ dòng điện (A), t là thời gian (giây), F là hằng số Faraday (96500 C/mol).
a) Giả thuyết của nhóm học sinh đưa ra là chính xác.
b) Tại mỗi thời điểm trong quá trình điện phân, khối lượng chìa khoá tăng lên bằng khối lượng đồng xu giảm đi.
c) Giá trị của m là 19,7.
d) Trên bề mặt của chìa khoá, xảy ra quá trình oxi hoá Cu thành ion Cu2+.
Câu trả lời tốt nhất
(a) Đúng, lượng chất thoát ra tại điện cực tỉ lệ thuận với cường độ dòng điện nên trong cùng một khoảng thời gian điện phân, nếu tăng cường độ dòng điện thì lượng đồng bám lên chìa khóa sẽ tăng.
(b) Sai, đồng xu là cực dương (anode), tại đó xảy ra quá trình oxi hóa:
Zn —> Zn2+ + 2e
Cu —> Cu2+ + 2e
Chìa khóa là cực âm (cathode), tại đó xảy ra quá trình khử:
Cu2+ + 2e —> Cu
Zn có phân tử khối lớn hơn Cu nên khối lượng đồng xu giảm sẽ nhiều hơn khối lượng chìa khóa tăng một chút.
(c) Đúng:
Từ đầu đến x phút:
mCu = 18,6 – 18,2 = 64I.60x/2F (1)
Từ x phút đến 2x phút:
mCu = 19,1 – 18,6 = 64(I + 0,5).60x/2F (2)
(1)/(2) —> 0,8 = I/(I + 0,5) —> I = 2A
(1) —> x ≈ 10 phút
Từ 2x phút đến 3x phút:
mCu = m – 19,1 = 64(I + 1).60x/2F —> m = 19,7 gam
(d) Sai, trên bề mặt chìa khóa xảy ra quá trình khử Cu2+ thành Cu.
