Phương pháp Solvay được sử dụng rộng rãi để sản xuất lượng lớn soda (Na2CO3) trong công nghiệp. Phương pháp này được minh họa như sơ đồ dưới đây:
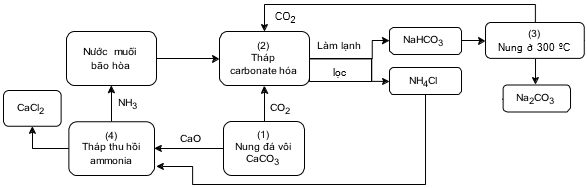
a) Soda được tạo ra từ NaHCO3 ở (3) bằng phản ứng nhiệt phân.
b) Trong thực tế, người ta còn sử dụng BaCO3 thay cho CaCO3 ở (1).
c) Sản phẩm NH4Cl sau khi ra khỏi tháp carbonate hóa (2) còn được tách ra để sử dụng làm phân đạm.
d) Để tiết kiệm chi phí, có thể thay thế dung dịch NaCl bão hòa bằng nước biển đã loại bỏ chất bẩn.
e) Giai đoạn sản xuất NaHCO3 từ NaCl, NH3, CO2, H2O có hiệu suất là 60%, NaHCO3 sinh ra được dùng để sản xuất thuốc giảm đau dạ dày. Một viên thuốc giảm đau dạ dày do chứng dư acid nặng 1 gam chứa 35% NaHCO3 về khối lượng. Để sản xuất được 2 triệu viên thuốc loại này cần 344 m³ CO2 (đkc, kết quả làm tròn đến hàng đơn vị).
Câu trả lời tốt nhất
(a) Đúng:
2NaHCO3 (t°) —> Na2CO3 + CO2 + H2O
(b) Sai, BaCO3 hiếm hơn và khó nhiệt phân hơn CaCO3 nên không sử dụng BaCO3 thay cho CaCO3 ở (1).
(c) Sai, theo chu trình khép kín thì NH4Cl chỉ vừa đủ để cung cấp NH3 cho phản ứng tổng hợp, vì vậy người ta không lấy NH4Cl ra, thậm chí phải bù đắp phần nhỏ bị hao hụt.
(d) Sai, nước biển có nồng độ NaCl chưa bão hòa, quá loãng sẽ ngăn NaHCO3 kết tinh, mặt khác nước biển ngoài NaCl còn chứa nhiều muối khác nên sản phẩm cuối cùng sẽ có độ tinh khiết thấp.
(e) Đúng:
NaCl + NH3 + H2O + CO2 → NH4Cl + NaHCO3
mNaHCO3 = 2000000.1.35% = 700000 gam = 700 kg
—> nCO2 = 700/(84.60%) = 125/9 kmol
—> V CO2 = 24,79.125/9 = 344 m³
