Mỗi amino acid có một pH cụ thể mà tại đó nồng độ của dạng zwitterionic (phân tử chứa cả điện tích dương và điện tích âm, tổng điện tích hình thức của nó bằng không) đạt giá trị cực đại. Độ pH này được gọi là độ pH đẳng điện hoặc điểm đẳng điện, kí hiệu là pI. Đối với amino acid không có chuỗi bên có tính acid hoặc tính base, pI chỉ đơn giản là giá trị trung bình của hai giá trị pKa. Đối với các amino acid có chuỗi bên có tính acid hoặc tính base, pl là giá trị trung bình của hai giá trị pKa tương ứng với các nhóm tương tự.
Một amino acid mang điện tích dương (dạng cation) trong dung dịch acid (pH thấp) và mang điện tích âm (dạng anion) trong dung dịch base (pH cao). Bằng cách thay đổi độ pH của dung dịch, chúng ta có thể kiểm soát điện tích trên phân tử. Khả năng kiểm soát điện tích của một amino acid này hữu ích để tách và xác định các amino acid bằng phương pháp điện di. Cho đồ thị biểu diễn đường cong chuẩn độ của glycine (hình bên).
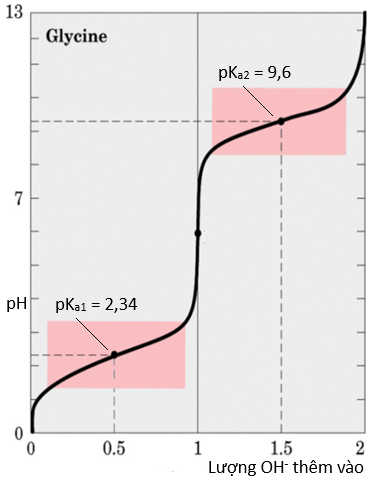
i. Tính giá trị pl của glycine.
ii. Viết công thức cấu tạo dạng tồn tại chủ yếu của glycine trong môi trường có các giá trị pH sau: pH < 2,34; 2,34 < pH < 9,6 và pH > 9,6.
Câu trả lời tốt nhất
i. Glycine có 1NH2, 1COOH, không có chức khác nên:
pI = (pKa1 + pKa2)/2 = 5,97
ii. Các dạng tồn tại chủ yếu của Glycine:
pH < 2,34: +H3N-CH2-COOH (1)
2,34 < pH < 9,6: +H3N-CH2-COO- (2)
pH > 9,6: H2N-CH2-COO- (3)

