Một pin điện hóa Ni-H2 được thiết lập như hình vẽ, vôn kế được sử dụng để đo sức điện động của pin ở điều kiện chuẩn.
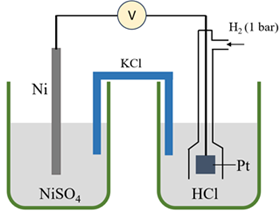
Cho thế điện cực chuẩn của cặp Ni2+/Ni bằng −0,257V. Phát biểu nào sau đây đúng?
A. Ở anode xảy ra quá trình oxi hóa Ni, ở cathode xảy ra quá trình khử H+.
B. Từ cầu muối, ion K⁺ đi vào dung dịch NiSO4, ion Cl- đi vào dung dịch HCl.
C. Suất điện động chuẩn của pin đo được là −0,257V.
D. Khối lượng điện cực Ni tăng dần, khối lượng điện cực Pt không đổi.
Câu trả lời tốt nhất
A. Đúng:
+ Tại anode: Ni —> Ni2+ + 2e
+ Tại cathode: 2H+ + 2e —> H2
B. Sai, từ cầu muối ion Cl- đi vào dung dịch NiSO4, ion K+ đi vào dung dịch HCl để cân bằng điện tích.
C. Sai, E°Ni-H2 = -(-0,257) = 0,257V
D. Sai, Ni tan dần nên khối lượng điện cực Ni giảm dần, không có gì bám vào nên khối lượng điện cực Pt không đổi.

