Một học sinh tiến hành thí nghiệm khảo sát mức độ phản ứng của các kim loại khác nhau (Cobalt, Magnesium, Zinc) với hydrochloric acid (HCl) bằng cách đo sự gia tăng nhiệt độ của dung dịch sau phản ứng. Học sinh tiến hành như sau:
• Bước 1: Đong 50 cm³ dung dịch HCl vào cốc polystyrene. Đo và ghi lại nhiệt độ ban đầu của acid.
• Bước 2: Thêm một lượng bột kim loại cố định (một thìa) vào cốc chứa acid. Khuấy đều để đảm bảo phản ứng xảy ra hoàn toàn. Quan sát và ghi lại nhiệt độ cao nhất của dung dịch sau phản ứng.
• Bước 3: Tính mức tăng nhiệt độ bằng cách lấy nhiệt độ cao nhất trừ đi nhiệt độ ban đầu. Lặp lại các bước trên thêm ba lần cho mỗi kim loại để đảm bảo kết quả chính xác. Tính giá trị trung bình của mức tăng nhiệt độ cho mỗi kim loại.
Kết quả của học sinh:
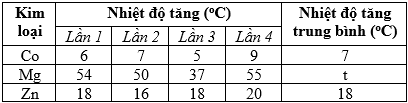
a) Thí nghiệm trên đạt được mục tiêu với giả thuyết: “kim loại hoạt động mạnh hơn sẽ tạo ra phản ứng với hydrochloric acid mãnh liệt hơn, dẫn đến sự gia tăng nhiệt độ lớn hơn”.
b) Nhiệt độ tăng trung bình của kim loại Magnesium trong thí nghiệm của học sinh có giá trị t = 50°C.
c) Lượng kim loại thêm vào mỗi lần không cần phải cố định, vì điều đó không ảnh hưởng đến kết quả do tốc độ phản ứng không thay đổi.
d) Kết quả thí nghiệm cho thấy Zinc phản ứng với dung dịch HCl mạnh hơn kim loại cobalt.
Câu trả lời tốt nhất
(a) Sai, thí nghiệm trên không đạt được mục tiêu vì không cùng điểm xuất phát. Thí nghiệm định lượng nhưng lại dùng kiểu áng chừng “mỗi kim loại một thìa” là không thể chấp nhận. Cứ cho rằng thể tích kim loại qua 12 lượt lấy là như nhau, do Zn, Co có khối lượng riêng rất lớn, Mg có khối lượng riêng rất nhỏ thì nMg sẽ gấp nhiều lần nZn, nCo, khi đó sẽ nảy sinh vấn đề: Mg tỏa nhiệt nhiều hơn do số mol nó lớn hơn chứ chắc gì nó đã mạnh hơn?
Để so sánh, xuất phát điểm phải giống nhau: cùng số mol, cùng kích cỡ hạt bột, cùng tình trạng (bột mới như nhau), cùng dùng HCl dư và nên giảm quy mô thí nghiệm để rút ngắn thời gian phản ứng (dùng ít hóa chất lại), thời gian càng ngắn, nhiệt tỏa ra ngoài càng ít, sai số càng nhỏ.
(b) Sai, t = (54 + 50 + 37 + 55)/4 = 49°C.
(c) Sai, lượng kim loại mỗi lần thêm phải giống nhau (về số mol) vì lượng nhiệt sinh ra phụ thuộc vào mol kim loại đã dùng.
(d) Sai, do thí nghiệm sai ngay từ đầu nên không kết luận được điều gì từ kết quả thí nghiệm.

