Trong công nghiệp hiện đại, quy trình Solvay đang được cải tiến theo hướng công nghệ xanh, kết hợp thu hồi CO2 (CCUS – Carbon Capture, Utilization and Storage) từ khí thải nhà máy nhiệt điện để cắt giảm khí phát thải. Ngoài ra, người ta còn nghiên cứu tận dụng CaCl2 (phụ phẩm) làm vật liệu chống băng hoặc hút ẩm. Quy trình gồm các phản ứng chính theo sơ đồ sau đây:
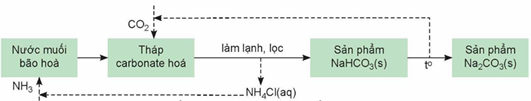
a) Phản ứng trong tháp carbonate hóa có thể biểu diễn gộp thành: 2NaCl + 2NH3 + CO2 + H2O → Na2CO3↓ + 2NH4Cl nên không cần xét đến sự tạo thành trung gian NaHCO3.
b) Biết độ tan của NaHCO3 ở 40°C và 20°C lần lượt là 12,7 và 9,6. Làm lạnh 100 tấn dung dịch bão hoà ở 40°C xuống 20°C, khối lượng NaHCO3 kết tinh là 2,48 tấn (giả thiết nước không bay hơi, kết quả làm tròn đến hàng phần trăm).
c) Trong toàn bộ quy trình Solvay cải tiến, NH3 và CO2 đều được tuần hoàn hoàn toàn nên về mặt cân bằng vật chất, hai chất này không phải là nguyên liệu tiêu hao.
d) Trong quy trình cải tiến, CaO thu được từ nhiệt phân đá vôi không chỉ dùng để tái sinh NH3 mà còn có thể dùng để hấp thụ CO2 dư tạo lại CaCO3 góp phần cắt giảm khí thải.
Câu trả lời tốt nhất
(a) Sai, phản ứng như vậy không xảy ra vì Na2CO3 tan tốt ngay cả ở nhiệt độ thấp. Các quá trình tạo NaHCO3 và Na2CO3 phải tách rời nhau:
NaCl + NH3 + CO2 + H2O → NaHCO3↓ + NH4Cl
2NaHCO3 —> Na2CO3 + CO2 + H2O
(b) Sai
mNaHCO3 kết tinh = x tấn, bảo toàn khối lượng NaHCO3:
100.12,7/(100 + 12,7) = x + (100 – x).9,6/(100 + 9,6)
—> x = 2,75
(c) Sai, nếu không tính hao hụt thì chỉ NH3 không bị tiêu hao, còn CO2 nằm lại một nửa trong Na2CO3 nên phải bù thêm liên tục theo từng chu kỳ sản xuất.
(d) Sai, CO2 từ nhiệt phân NaHCO3 và CaCO3 không dư (thậm chí còn thiếu nếu bị hao hụt), vì vậy CaO chỉ làm nhiệm vụ tách NH3 từ NH4Cl.
