Acquy chì khi phóng điện được mô tả theo mô hình bên:
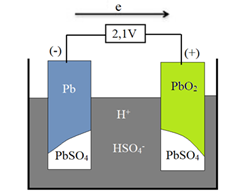
Tại anode (cực âm): Pb(s) + HSO4-(aq) → PbSO4(s) + H+(aq) + 2e
Tại cathode (cực dương): PbO2(s) + HSO4-(aq) + 3H+(aq) + 2e → PbSO4(s) + 2H2O(l)
Trong quá trình acquy phóng điện, sự thay đổi nào sau đây đúng?
A. Khối lượng các điện cực tăng.
B. Nồng độ H+ trong dung dịch tăng.
C. Nồng độ H2SO4 trong dung dịch tăng.
D. Sức điện động (E) của acquy tăng.
Câu trả lời tốt nhất
A. Đúng, khối lượng các điện cực tăng do sự thay đổi thành phần chất rắn: ở anode (Pb —> PbSO4, tăng 96 gam/mol), ở cathode (PbO2 —> PbSO4, tăng 64 gam/mol).
B. Sai, nồng độ H+ trong dung dịch giảm do anode sinh ra 1 mol H+ thì cathode lại tiêu thụ 3 mol H+.
C. Sai, H2SO4 chuyển hóa thành kết tủa PbSO4 nên nồng độ giảm.
D. Sai, sức điện động (E) của acquy giảm dần do nồng độ H2SO4 giảm dần, các điện cực dần bị bao phủ bởi PbSO4 làm tiếp xúc điện kém, các chất phản ứng hao hụt dần làm phản ứng chậm dần.

