Aspirin (hay acetylsalicylic acid), là một dẫn xuất của salisylic acid được sử dụng để hạ sốt và giảm đau nhẹ đến trung bình do tình trạng đau nhức cơ, răng, cảm lạnh đau đầu và sưng tấy do viêm khớp. Một nhóm học sinh thực hiện tổng hợp Aspirin trong phòng thí nghiệm như sau:
Bước 1: Cho 75,0 gam salicylic acid khan và 105,0 ml acetic nhydride (d = 1,08 g/mL) vào bình cầu 250 ml; thêm 4,0 ml sulfuric acid đặc vào và lắc kĩ. Sau đó, khuấy khối phản ứng ở 50 – 60°C trong khoảng 45 phút cho đến khi tan hết phần chất rắn.
Bước 2: Dùng nước đá để làm lạnh hỗn hợp phản ứng đến nhiệt độ nhỏ hơn 10°C. Cho hỗn hợp vào cốc lớn, thêm từ từ 750 ml nước cất và khuấy kỹ, aspirin sẽ kết tủa. Lọc lấy sản phẩm bằng phễu lọc Buchner.
Bước 3: Hòa tan aspirin thô trong 100 ml ethanol 90°, đun nóng để tan hoàn toàn, sau đó đổ dung dịch này từ từ vào 450 ml nước nóng khoảng 50°C, đun nóng nhẹ cho chất rắn tan hết. Để nguội dung dịch thu được đến nhiệt độ phòng. Aspirin kết tinh dưới dạng tinh thể, lọc và hút hết nước, sây khô ở 50°C.
Bước 4: Cân sản phẩm thu được 83,1 gam aspirin.
Biết phương trình hóa học điều chế aspirin từ salicylic acid được biểu diễn như sau:
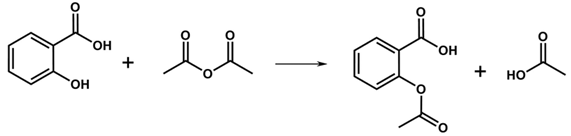
a. Phương pháp tách và tinh chế aspirin ở trên là phương pháp kết tinh.
b. Aspirin tan trong nước nhiều hơn salicylic acid.
c. Hiệu suất của quá trình tổng hợp aspirin ở thí nghiệm trên đạt khoảng 85%.
d. Aspirin là hợp chất hữu cơ tạp chức, trong đó có chức ester và chức phenol.
Câu trả lời tốt nhất
(a) Đúng
(b) Sai, aspirin có chức ester nên tan trong nước kém hơn salicylic acid.
(c) Đúng
nHOC6H4COOH = 75/138 = 0,54348 mol
n(CH3CO)2O = 105.1,08/102 = 1,11176 mol
nCH3COOC6H4COOH = 83,1/180 = 0,46167 mol
—> H = 0,46167/0,54348 = 85%
(d) Sai, aspirin là hợp chất hữu cơ tạp chức, trong đó có chức ester và chức carboxylic.

