Calcium carbonate là thành phần chính có trong vỏ trứng, vỏ sò, vỏ ốc,… Để xác định hàm lượng calcium carbonate có trong một mẫu vỏ trứng, một nhóm học sinh đã làm như sau:
– Bước 1: Rửa sạch vỏ trứng bằng nước cất, sấy cho đến khi khô hoàn toàn rồi nghiền thành bột.
– Bước 2: Cân chính xác 2,2 gam bột vỏ trứng rồi cho vào bình nón. Thêm 100,0 mL dung dịch hydrochloric acid 2,0M vào bình nón, đậy hờ và để trong vài giờ.
– Bước 3: Lọc dung dịch trong bình nón cho vào bình định mức 250,0 mL rồi thêm nước cất đến vạch và lắc đều.
– Bước 4: Cho dung dịch sodium hydroxide 1,0M vào burette 50,0 mL và điều chinh dung dịch trong burette về mức 0.
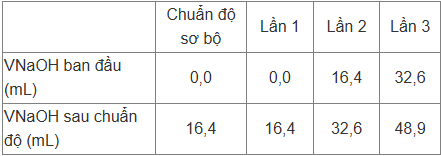
– Bước 5: Chuyển 25,0 mL dung dịch đã chuẩn bị ở bước 3 vào bình nón, thêm vài giọt chất chỉ thị acid – base thích hợp và tiến hành chuần độ. Học sinh đã thực hiện chuẩn độ sơ bộ (bước thử trước khi chuẩn độ chính thức) rồi lặp lại chuẩn độ 3 lần nữa, kết quả thí nghiệm được ghi lại trong bảng sau:
a) Viết phương trình hóa học của các phản ứng xảy ra.
b) Nêu vai trò của lần chuẩn độ sơ bộ.
c) Đưa ra 2 lý do vì sao không chuẩn độ trực tiếp calcium carbonate trong vỏ trứng bằng dung dịch HCl.
d) Học sinh lặp lại thí nghiệm chuẩn độ bằng cùng một thiết bị nhưng sử dụng dung dịch NaOH 0,10M. Giải thích lý do tại sao điều này lại gây ra hạn chế cho quy trình chuẩn độ.
e) Tính hàm lượng calcium carbonate trong mẫu vỏ trứng.
Câu trả lời tốt nhất
(a) CaCO3 + 2HCl —> CaCl2 + CO2 + H2O
NaOH + HCl —> NaCl + H2O
(b) Chuẩn độ sơ bộ là phép thử giúp người làm đánh giá xem thể tích dung dịch NaOH tiêu tốn khoảng bao nhiêu khi kết thúc chuẩn độ, từ đó xác định nồng độ NaOH chuẩn hay sức chứa burette đã phù hợp hay chưa.
(c) Không chuẩn độ trực tiếp calcium carbonate trong vỏ trứng bằng dung dịch HCl vì:
+ CaCO3 không tan, không có chất chỉ thị phù hợp và khó kiểm soát điểm kết thúc.
+ CaCO3 phân bố đều trong vỏ trứng cùng nhiều tạp chất khác nên quá trình hòa tan trong HCl rất chậm (mất vài giờ).
(d) Sau lần chuẩn độ sơ bộ, thấy tiêu tốn khoảng 16,4 mL dung dịch NaOH 1M. Nếu dùng dung dịch NaOH 0,1M, thể tích lúc này sẽ là 164 mL, vượt quá sức chứa của burette đang sử dụng (50 mL). Nếu giảm dung dịch trong bình tam giác xuống 2,5 mL, sai số sẽ lớn.
(e) VddNaOH trung bình = [(16,4 – 0) + (32,6 – 16,4) + (48,9 – 32,6)]/3 = 16,3 mL
nHCl dư (25 mL) = nNaOH = 16,3.1 = 16,3 mmol
nHCl dư (250 mL) = 163 mmol = 0,163 mol
nHCl ban đầu = 0,2 —> nHCl phản ứng với CaCO3 = 0,037
—> nCaCO3 = 0,0185 —> %CaCO3 = 0,0185.100/2,2 = 84,09%
