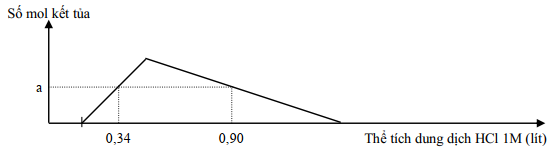
Cho 49,2 gam hỗn hợp gồm Ba, BaO, Al và Al2O3 vào nước dư, thu được 0,24 mol khí H2 và dung dịch X. Cho dung dịch HCl 1M đến dư vào X, sự phụ thuộc số mol kết tủa và thể tích dung dịch HCl 1M được biểu diễn theo đồ thị sau:
Nếu cho từ từ V ml dung dịch HCl 0,4M và H2SO4 0,6M vào X, thì thu được kết tủa lớn nhất. Giá trị của V là
A. 300. B. 450. C. 600. D. 400.
Câu trả lời tốt nhất
Quy đổi hỗn hợp ban đầu thành Ba (b), Al (c) và O.
Bảo toàn electron: 2b + 3c = 2nO + 2nH2
—> nO = b + 1,5c – 0,24
—> 137b + 27c + 16(b + 1,5c – 0,24) = 49,2 (1)
Dung dịch X chứa Ba2+ (b), AlO2- (c), bảo toàn điện tích —> 2b – c
nH+ = 0,34 = (2b – c) + a (2)
nH+ = 0,90 = (2b – c) + 4c – 3a (3)
(1)(2)(3) —> a = 0,18; b = 0,24; c = 0,32
Vậy X chứa Ba2+ (0,24), AlO2- (0,32), OH- (0,16)
nHCl = 0,4V và nH2SO4 = 0,6V —> nH+ = 1,6V
Khi BaSO4 max thì 0,6V = 0,24 —> V = 0,4
—> nH+ = 0,64
nH+ = nOH- + 4nAlO2- – 3nAl(OH)3 —> nAl(OH)3 = 4/15
—> m↓ = 76,72
Khi Al(OH)3 max thì nH+ = 1,5V = nOH- + nAlO2-
—> V = 0,32
—> nSO42- = 0,192 —> nBaSO4 = 0,192
—> m↓ = 69,696 < 76,72
Vậy m↓ max = 76,72 khi V = 0,4 lít
