Cho biểu đồ nhiệt độ sôi (°C) của một số chất như sau:
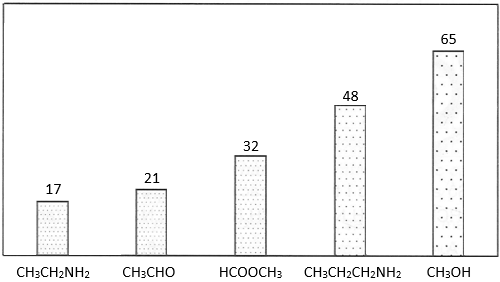
Câu 17. Từ biểu đồ về nhiệt độ sôi, phát biểu nào sau đây đúng?
A. Propan-1-amine có nhiệt độ sôi cao hơn ethanamine do tạo được nhiều liên kết hydrogen hơn.
B. Ethanamine có nhiệt độ sôi thấp nhất do không tạo được liên kết hydrogen liên phân tử.
C. Methanol có nhiệt độ sôi cao hơn ethanamine, propan-1-amine do liên kết hydrogen giữa các phân tử alcohol bền hơn amine.
D. Sự khác nhau về nhiệt độ sôi của ethanamine và propan-1-amine không bị ảnh hưởng bởi tương tác van der Waals giữa các phân tử.
Câu 18. Số chất là chất khí ở điều kiện chuẩn (25°C, 1 bar) là:
A. 4. B. 1. C. 5. D. 2.
Câu trả lời tốt nhất
Câu 17.
A. Sai, propan-1-amine có nhiệt độ sôi cao hơn ethanamine chủ yếu là do khối lượng phân tử lớn hơn và tương tác van der Waals mạnh hơn. Cả hai đều là amine bậc 1 và chỉ có một nhóm -NH2, nên khả năng tạo số lượng liên kết hydrogen trên mỗi phân tử là tương đương nhau. Sự chênh lệch nhiệt độ sôi ở đây không phải do “tạo được nhiều liên kết hydrogen hơn”.
B. Sai, mặc dù ethanamine có nhiệt độ sôi thấp nhất trong dãy, nhưng lý do phát biểu đưa ra là sai. Ethanamine là amine bậc 1, nó có tạo được liên kết hydrogen liên phân tử (giữa nguyên tử H linh động của nhóm -NH2 và nguyên tử N của phân tử khác). Nó có nhiệt độ sôi thấp hơn CH3CHO hay HCOOCH3 trong dãy này chủ yếu vì khối lượng phân tử của nó nhỏ nhất và liên kết hydrogen của amine yếu hơn của alcohol.
C. Đúng, liên kết O-H phân cực mạnh hơn liên kết N-H (do độ âm điện của O > N). Vì vậy, liên kết hydrogen giữa các phân tử alcohol bền vững hơn nhiều so với liên kết hydrogen giữa các phân tử amine.
D. Sai, tương tác van der Waals phụ thuộc rất lớn vào khối lượng phân tử và diện tích bề mặt tiếp xúc. Propan-1-amine có mạch carbon dài hơn ethanamine, dẫn đến lực van der Waals lớn hơn. Đây chính là yếu tố gây ra sự khác biệt về nhiệt độ sôi khi cả hai đều có cùng kiểu liên kết hydrogen.
Câu 18.
Có 2 chất khí ở điều kiện chuẩn (25°C, 1 bar) là CH3CH2NH2 và CH3CHO.
