Cho pin điện hoá có cấu tạo như sau:
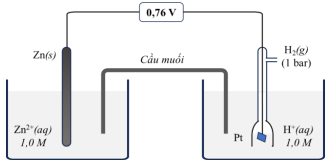
a) Thế điện cực chuẩn E°Zn2+/Zn = −0,76V
b) Khi pin hoạt động, ion âm trong cầu muối di chuyển về phía điện cực hydrogen.
c) Tại điện cực dương xảy ra quá trình khử ion H+(aq) thành khí H2(g).
d) Phản ứng xảy ra trong pin là: H2(g) + Zn2+(aq) → Zn(s) + 2H+(aq).
Câu trả lời tốt nhất
(a) Đúng: E°pin = E°2H+/H2 – E°Zn2+/Zn = 0,76V
E°2H+/H2 = 0 —> E°Zn2+/Zn = -0,76V
(b) Sai, khi pin hoạt động, ion âm trong cầu muối di chuyển về phía điện cực Zn để trung hòa điện tích dương của Zn2+ vừa sinh ra thêm.
(c) Đúng, tại cực dương: 2H+ + 2e —> H2
(d) Sai, phản ứng xảy ra trong pin là: Zn(s) + 2H+(aq) → H2(g) + Zn2+(aq).
×

