Cho từ từ đến dư dung dịch H2SO4 vào dung dịch chứa NaAlO2 và BaCl2. Khối lượng kết tủa (y gam) phụ thuộc vào số mol H2SO4 (x mol) theo đồ thị như hình vẽ.
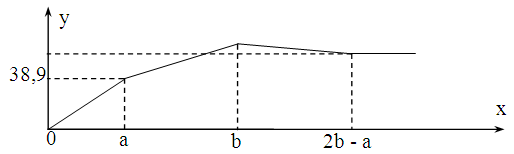
Khối lượng kết tủa cực đại là
A. 108,8 gam B. 73,85 gam. C. 58,25 gam. D. 66,05 gam.
Câu trả lời tốt nhất
Đoạn 1: Tạo đồng thời 2 kết tủa:
H+ + H2O + AlO2- —> Al(OH)3
SO42- + Ba2+ —> BaSO4
—> nAl(OH)3 = 2a và nBaSO4 = a
—> m↓ = 78.2a + 233a = 38,9
—> a = 0,1
Đoạn 2: Khi Al(OH)3 bị hòa tan hết thì mBaSO4 > 38,9 —> Trong đoạn này BaSO4 tiếp tục được tạo ra, đồng thời Al(OH)3 bị hòa tan một phần.
—> nNaAlO2 = 2a = 0,2 và nBaCl2 = b
Đoạn 3: Chỉ còn phản ứng hòa tan Al(OH)3 đến hết:
nH+ = 4nAlO2- ⇔ 2(2b – a) = 4.0,2
—> b = 0,25
Quay trở lại đoạn 2:
nBaSO4 max = b = 0,25
nH+ = 2b = 4nAlO2- – 3nAl(OH)3 —> nAl(OH)3 = 0,1
—> m↓ max = 66,05 gam
ad ơi tại sao gđ 2 ko tiếp tục tạo ra kết tủa al(oh)3 sau đó tan một phần ạ
