Cho từ từ dung dịch H2SO4 0,2M vào dung dịch chứa Ba(AlO2)2 0,1M và Ba(OH)2 0,2M. Khổi lượng kết tủa (m gam) phụ thuộc vào thê tích dung dịch H2SO4 (V ml) theo đồ thị sau:
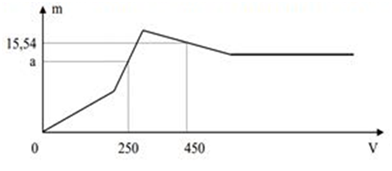
Giá trị của a là
A. 13,21. B. 12,43. C. 11,65. D. 13,98.
Câu trả lời tốt nhất
nBa(AlO2)2 = b và nBa(OH)2 = 2b
—> nBa2+ = 3b, nAlO2- = 2b và nOH- = 4b
Đoạn 1:
OH- + H+ —> H2O
Ba2+ + SO42- —> BaSO4
Đoạn 2:
AlO2- + H+ + H2O —> Al(OH)3
Ba2+ + SO42- —> BaSO4
Khi nH2SO4 = 0,05 —> nBaSO4 = 0,05 và nAl(OH)3 = 0,1 – 4b
—> m↓ = a = 0,05.233 + 78(0,1 – 4b) (1)
Đoạn 3:
Al(OH)3 + 3H+ —> Al3+ + 3H2O
nH2SO4 = 0,09 —> nH+ = 0,18 = nOH- + 4nAlO2- – 3nAl(OH)3
—> nAl(OH)3 = 4b – 0,06
—> m↓ = 233.3b + 78(4b – 0,06) = 15,54 (2)
(1)(2) —> a = 13,21 và b = 0,02
×
