Để điều chế một lượng nhỏ khí chlorine trong phòng thí nghiệm, người ta cho dung dịch HCl đặc phản ứng với MnO2 rắn theo sơ đồ dưới đây:
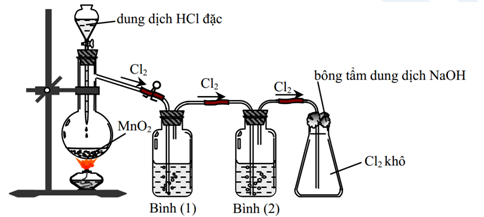
a) Bình (1) đựng dung dịch NaCl dùng để hòa tan 1 ít khí chlorine, bình (2) đượng H2SO4 đặc dùng để hút ẩm, làm khô khí, đảm bảo chất lượng chlorine.
b) Bông tẩm dung dịch NaOH giúp ngăn khí chlorine rò rỉ ra ngoài.
c) Nếu hoán đổi vị trí bình (1) và (2) thì chất lượng khí chlorine thu được sẽ không đổi.
d) Khi thay MnO2 ở thí nghiệm trên bằng KMnO4 cùng khối lượng thì lượng chlorine thu được sẽ nhiều hơn, biết HCl dùng dư, các phản ứng đều xảy ra hoàn toàn.
Câu trả lời tốt nhất
(a) Sai, bình 1 đựng dung dịch NaCl bão hòa để loại bỏ HCl lẫn trong Cl2. HCl tan tốt nên tan được trong dung dịch NaCl, Cl2 rất ít tan trong dung dịch NaCl bão hòa. Bình (2) đựng H2SO4 đặc dùng để hút ẩm.
(b) Đúng
(c) Sai, không thể hoán đổi bình (1) và (2), giai đoạn làm khô phải ở sau cùng. Nếu làm khô trước rồi lại dẫn qua dung dịch thì Cl2 sẽ bị ẩm.
(d) Đúng, cùng m gam thì KMnO4 nhận nhiều electron hơn MnO2 (5m/158 > 2m/87) nên Cl2 thoát ra nhiều hơn.
