Hiện nay người ta sản xuất ammonia theo chu trình Haber – Bosch bằng cách chuyển hoá có xúc tác một hỗn hợp gồm không khí, hơi nước và khí methane (trong các tháp phản ứng) qua các giai đoạn theo sơ đồ sau:
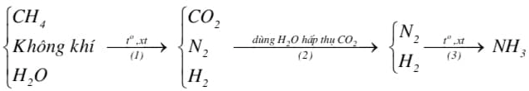
+ Viết các phương trình hóa học xảy ra trong các quá trình trên.
+ Nếu lấy 1000 m³ không khí (chứa 21% O2 và 78% N2, còn lại là CO2) thì cần phải lấy V m³ khí methane để thu được lượng N2 và H2 theo tỉ lệ 1 : 3 về thể tích dùng cho phản ứng tổng hợp ammonia. Biết các phản ứng ở giai đoạn (1) đều xảy ra hoàn toàn, các thể tích khí và hơi được đo ở cùng điều kiện.
b) Ở giai đoạn (3) xảy ra cân bằng: N2(g) + 3H2(g) ⇋ 2NH3(g)
– Tính  của phản ứng tổng hợp trên. Cho biết
của phản ứng tổng hợp trên. Cho biết  của NH3 là -45,9 kJ/mol.
của NH3 là -45,9 kJ/mol.
– Theo nguyên lý chuyển dịch cân bằng Le Chatelier, để tăng hiệu suất tổng hợp thì phản ứng nên được thực hiện ở nhiệt độ cao hay thấp? Vì sao?
– Trong thực tế, phản ứng được thực hiện ở nhiệt độ khá cao (khoảng 450°C). Hãy giải thích.
Câu trả lời tốt nhất
Phản ứng:
Giai đoạn 1:
CH4 + 2H2O → CO2 + 4H2 (1)
CH4 + 2O2 → CO2 + 2H2O (2)
Giai đoạn 2:
H2O + CO2 → H2CO3
Giai đoạn 3:
N2 + 3H2 ⇋ 2NH3
1000 m³ không khí chứa 210 m³ O2 và 780 m³ N2
—> V H2 = 780.3 = 2340 m³
(1) —> V CH4 = 2340.1/4 = 585 m³
(2) —> V CH4 = 210.1/2 = 105 m³
—> V CH4 tổng = 690 m³
(b)
 = -45,9.2 = -91,8 kJ
= -45,9.2 = -91,8 kJ
Phản ứng thuận tỏa nhiệt nên theo nguyên lý chuyển dịch cân bằng Le Chatelier, để tăng hiệu suất tổng hợp thì phản ứng nên được thực hiện ở nhiệt độ cao hay thấp, khi đó cân bằng sẽ chuyển dịch theo chiều thuận.
Trong thực tế, phản ứng được thực hiện ở nhiệt độ khá cao (khoảng 450°C) vì ở nhiệt độ thấp phản ứng lại không xảy ra.

