Hòa tan hết m gam hỗn hợp gồm Ba, BaO, Al và Al2O3 trong nước dư, thu được a mol khí H2 và dung dịch X. Cho dung dịch H2SO4 đến dư vào X, phản ứng được biểu diễn theo đồ thị sau:
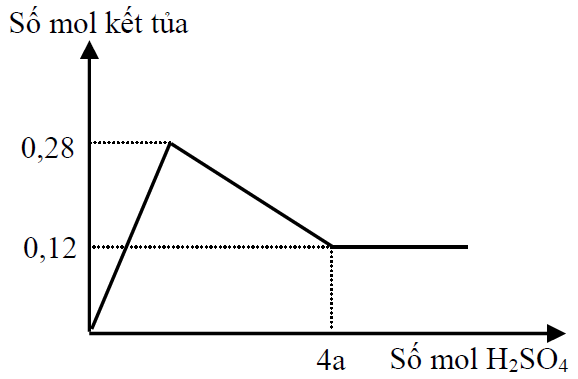
Giá trị của m là.
A. 26,52 gam. B. 25,56 gam.
C. 23,64 gam. D. 25,08 gam.
Câu trả lời tốt nhất
n↓ max = nBaSO4 + nAl(OH)3 = 0,28
nBaSO4 = 0,12 —> nAl(OH)3 = 0,16
Dung dịch X chứa Ba2+ (0,12), AlO2- (0,16) —> nOH- = 0,08
Để hòa tan hết Al(OH)3 thì:
nH+ = 8a = nOH- + 4nAlO2- —> a = 0,09
Ban đầu hỗn hợp chứa Ba (0,12), Al (0,16) và O. Bảo toàn electron:
0,12.2 + 0,16.3 = 2nO + 2nH2 —> nO = 0,27
—> m = 25,08
cho e hỏi các giai đoạn xảy ra như thế nào ạ
và vì sao nH+ = 8a ạ
cho e hỏi H+ + OH- ở đoạn nào vậy ạ trên đồ thị e thấy nó tạo kết tủa ngay lúc đầu
×

