Hòa tan hoàn toàn a gam hỗn hợp Al và Mg trong dung dịch HNO3 loãng. Kết thúc phản ứng, sản phẩm thu được gồm dung dịch X (không chứa muối amoni) và 0,084 mol hỗn hợp khí Y gồm N2 và N2O (không có sản phẩm khử nào khác của N+5). Tỉ khối hơi của Y so với H2 là 62/3. Cho từ từ từng giọt dung dịch NaOH 2M vào dung dịch X, thì lượng kết tủa thu được phụ thuộc vào lượng NaOH phản ứng được biểu thị bằng đồ thị dưới đây
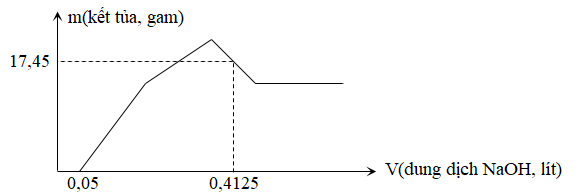
Giá trị của a là
A. 6,60. B. 6,30. C. 7,05. D. 7,50.
Câu trả lời tốt nhất
Y gồm N2 (0,014) và N2O (0,07)
Đặt x, y là số mol Al và Mg, bảo toàn electron:
3x + 2y = 0,014.10 + 0,07.8 (1)
Kết tủa bắt đầu xuất hiện khi nNaOH = 0,1 —> nH+ dư = 0,1
—> nNO3-(X) = 3x + 2y + 0,1 = 0,8
Khi nNaOH = 0,825 thì dung dịch thu được chứa Na+ (0,825), NO3- (0,8), bảo toàn điện tích —> nAlO2- = 0,025
—> m↓ = 78(x – 0,025) + 58y = 17,45 (2)
(1)(2) —> x = 0,1; y = 0,2
—> a = 27x + 24y = 7,5
