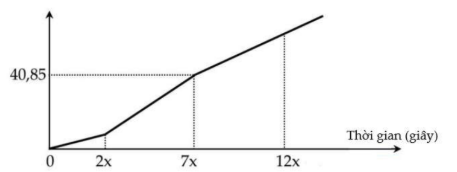
Hòa tan hoàn toàn hỗn hợp X gồm FeCl3, FeCl2, CuCl2 trong nước thu được dung dịch Y. Điện phân dung dịch Y bằng dòng điện một chiều với điện cực trơ. Đồ thị biểu diễn khối lượng dung dịch giảm theo thời gian như sau:
Nếu cho NaOH dư vào dung dịch đã điện phân phân được 10x giây thì thu được 31,5 gam kết tủa. Nếu điện phân dung dịch Y trong thời gian 12x giây sau đó cho AgNO3 dư vào dung dịch sau điện phân thì khối lượng kết tủa thu được gần nhất với:
A. 100. B. 99. C. 180. D. 170.
Câu trả lời tốt nhất
Cứ x giây thì lượng electron trao đổi tại các điện cực là a mol
Đoạn 1: Kéo dài 2x giây, tương ứng 2a mol electron.
2FeCl3 —> 2FeCl2 + Cl2
2a……………….2a……..a
Đoạn 2: Kéo dài 5x giây, tương ứng 5a mol electron.
CuCl2 —> Cu + Cl2
2,5a………..2,5a…..2,5a
Khi kết thúc đoạn 2:
m giảm = 71(a + 2,5a) + 64.2,5a = 40,85
—> a = 0,1
Đoạn 3, thời điểm 10x giây còn lại nFeCl2 = nFe(OH)2 = 0,35 mol
Thời điểm 12x giây, tức là điện phân thêm 2x giây nữa (Trao đổi 0,2 mol electron nữa) thì còn lại:
nFeCl2 = 0,35 – 0,2/2 = 0,25
—> nAg = 0,25 và nAgCl = 0,5
—> m↓ = 98,75
Cho em hỏi nếu viết theo dạng ion điện phân tại 2 cực ấy ạ , tại đoạn gấp khúc đầu tiên có thể cho rằng cl- hết không ạ ?

