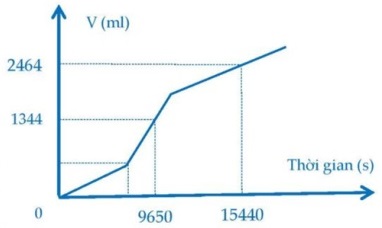
Hòa tan m gam hỗn hợp CuSO4 và NaCl vào nước được dung dịch X. Điện phân dung dịch X bằng dòng điện một chiều có cường độ 1,0A (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước). Tổng thể tích khí (đktc) thu được ở cả hai điện cực (ml) phụ thuộc vào thời gian điện phân (t) được mô tả như đồ thị hình bên.
Cho các phát biểu sau về quá trình điện phân trên
(a) Tại thời điểm H2O bắt đầu bị điện phân ở cả 2 điện cực, số mol khí thu được ở anot là 0,08 mol.
(b) Khi thời gian điện phân là 9650 giây, khối lượng chất thoát ra ở catot là 2,58 gam.
(c) Giá trị của m là 13,42 gam.
(d) Khi H2O bắt đầu bị điện phân ở cả 2 điện cực thì thời gian điện phân là 12250 (giây).
(e) Dung dịch thu được sau điện phân hòa tan tối đa 1,08 gam Al.
Số phát biểu đúng là
A. 1. B. 4. C. 3. D. 2.
Câu trả lời tốt nhất
Đoạn 1 thoát khí Cl2. Đoạn 2 có độ dốc lớn hơn nên tốc độ thoát khí nhanh hơn (Cl2, H2). Đoạn 3 thoát khí O2, H2.
Khi t = 9650 thì ne = 0,1 —> nCl2 = 0,05
n khí tổng = 0,06 —> nH2 = 0,06 – 0,05 = 0,01
Bảo toàn electron cho catot —> nCuSO4 = nCu = 0,04
Khi t = 15440 thì ne = 0,16
Catot: nCu = 0,04 —> nH2 = 0,04
Anot: nCl2 = u và nO2 = v
—> n khí tổng = u + v + 0,04 = 0,11
ne = 2u + 4v = 0,16
—> u = 0,06; v = 0,01
(a) Sai, khi H2O bắt đầu bị điện phân ở 2 điện cực thì n khí anot = nCl2 = 0,06
(b) Đúng, ở catot thoát ra mCu + mH2 = 0,04.64 + 0,01.2 = 2,58 gam.
(c) Đúng, nCuSO4 = 0,04; nNaCl = 2u = 0,12 —> m = 13,42 gam
(d) Sai, H2O bắt đầu bị điện phân ở 2 điện cực khi ne = 2u = It/F —> t = 11580s
(e) Đúng, dung dịch sau điện phân chứa nOH- = 0,12 – 0,04.2 = 0,04 —> nAl = 0,04 —> mAl = 1,08 gam
