Kẽm (zinc) là kim loại có nhiều ứng dụng trong công nghiệp như mạ kẽm chống ăn mòn, sản xuất hợp kim,… đồng thời kẽm còn là một vi chất thiết yếu cho sự sống. Lượng kẽm này được tách chủ yếu từ quặng zinc blende (ZnS) theo các bước sau:
• Bước 1. Làm giàu quặng: Quặng được nghiền nhỏ và cho vào nước có thổi không khí. Các hạt đất, đá lắng xuống đáy, zinc sulfide nổi lên cùng với bọt. Lớp bọt này được tách ra và sấy khô.
• Bước 2. Đốt quặng: Nung nóng zinc sulfide trong lò thu được zinc oxide.
2ZnS + 3O2 → 2ZnO + 2SO2
• Bước 3. Khử zinc oxide: ZnO được trộn với than cốc và nung ở nhiệt độ 1400°C: ZnO + C → Zn + CO
• Bước 4. Thu hồi: Kim loại kẽm tạo thành được làm nguội, khí CO sinh ra được đốt cháy, nhiệt lượng tỏa ra giúp giảm chi phí vận hành lò nung.
Biết rằng: kẽm có khối lượng riêng bằng 7,13 g/cm³, nóng chảy ở 419,5°C, sôi ở 906°C.
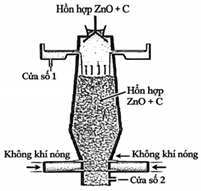
Câu 15. Phát biểu nào dưới đây đúng?
A. Khí SO2 từ nhà máy nếu không qua xử lí sẽ gây ô nhiễm môi trường nước.
B. Kẽm được tách ra theo phương pháp oxy hoá – khử trong dung dịch.
C. Quá trình thổi không khí vào hỗn hợp bột quặng và nước (bước 1) xảy ra biến đổi hoá học.
D. Cửa số (2) trong sơ đồ lò nung thu được hỗn hợp khí CO và CO2.
Câu 16. Đồng thau là hợp kim của khoảng 70% đồng và 30% kẽm. Hợp kim này tan hoàn toàn trong dung dịch nào dưới đây?
A. Dung dịch NaCl. B. Dung dịch CuCl2.
C. Dung dịch HNO3. D. Dung dịch HCl.
Câu 17. Cho các nhận định sau về sản xuất và ứng dụng của kẽm:
(1) Trong mạ kẽm chống ăn mòn thép, kẽm là lớp bảo vệ bề mặt, đồng thời bảo vệ điện hoá cho thép.
(2) Cả hai phản ứng xảy ra tại bước 2 và bước 3 trong sơ đồ đều là phản ứng oxi hoá – khử.
(3) Khí thải từ bước 2 và bước 3 đều là nguyên nhân trực tiếp gây mưa axit.
(4) Kẽm được thu hồi ở bước 4 dạng lỏng (cửa số 1) do kẽm là kim loại nặng.
(5) Nhiệt độ của lò nung được cung cấp bởi đốt cháy carbon và đốt cháy khí CO.
Số phát biểu đúng là
A. 5. B. 2. C. 3. D. 4.
Câu 18. Phương pháp tách kim loại nào đã được sử dụng trong bước 3 của sơ đồ trên?
A. Điện phân. B. Kết tinh.
C. Nhiệt luyện. D. Thuỷ luyện.
Câu trả lời tốt nhất
Câu 15.
A. Đúng, dù SO2 là một chất khí thường được nhắc đến như tác nhân gây ô nhiễm không khí, nhưng tác động của nó đối với hệ thống nước là cực kỳ nghiêm trọng. Có 2 con đường chuyển hóa SO2 vào nước là bị oxi hóa và theo nước mưa rơi xuống thành mưa acid hoặc trực tiếp hòa tan vào nước (nếu lâu ngày không có mưa). Tác động tới môi trường nước: tiêu diệt sinh vật thủy sinh, phá vỡ chuỗi thức ăn và hòa tan kim loại nặng từ các trầm tích (do tính acid mạnh).
B. Sai, kẽm được tách ra theo phương pháp nhiệt luyện.
C. Sai, quá trình làm giàu quặng ở bước 1 không xảy ra phản ứng do các hạt khoáng ZnS khó bị nước làm ướt, không khí được thổi vào để tạo bọt và cuốn các hạt ZnS nổi lên cùng lớp bọt.
D. Sai, tất cả các chất khí sẽ thu từ đỉnh lò theo nguyên tắc đối lưu. Các khí CO, CO2, Zn thoát ra được làm mát tại các đĩa ở phía trên, Zn nhanh chóng hóa lỏng và tách ra ở cửa 1. Cửa số 2 dưới đáy lò dùng để lấy xỉ, bao gồm tất cả các chất rắn còn dư, tạp chất không cháy…
Câu 16.
Đồng thau (hợp kim Cu-Zn) có thể tan hoàn toàn trong dung dịch HNO3, ví dụ:
3Zn + 8HNO3 —> 3Zn(NO3)2 + 2NO + 4H2O
3Cu + 8HNO3 —> 3Cu(NO3)2 + 2NO + 4H2O
Câu 17.
(1) Đúng, Zn phủ kín bề mặt thép nên Zn là kim loại bảo vệ bề mặt (giống như sơn hoặc dầu mỡ). Trong quá trình sử dụng, khi bề mặt bị xước, thủng thì Zn lại bảo vệ thép theo phương pháp điện hóa: Zn là anode, bị oxi hóa; thép là cathode, được bảo vệ.
(2) Đúng
(3) Sai, khí thải SO2 là nguyên nhân gây mưa acid. Khí thải CO không gây mưa acid.
(4) Sai, Zn là kim loại nặng không phải là lý do. Phản ứng tỏa nhiều nhiệt nên Zn sinh ra ở dạng khí, sau đó làm lạnh thì ngưng tụ thành dạng lỏng và tự tách khỏi CO, CO2 (vẫn ở dạng khí).
(5) Đúng, phản ứng đốt cháy ZnS tỏa nhiệt, phản ứng khử ZnO thu nhiệt, tuy nhiên chúng không thể tự cân đối mà vẫn thiếu rất nhiều nhiệt do lò nung đòi hỏi duy trì ở nhiệt độ cao. Đốt cháy C và CO sẽ bổ sung lượng nhiệt cần thiết còn thiếu.
Câu 18.
Phương pháp nhiệt luyện đã được sử dụng trong bước 3 của sơ đồ trên.
