Một nhóm học sinh làm thí nghiệm để nghiên cứu sự phụ thuộc của sức điện động vào nồng độ của ion kim loại. Giả thuyết mà nhóm học sinh này đặt ra là: “Khi giảm nồng độ ion kim loại trong dung dịch thì sức điện động của pin cũng giảm”. Để kiểm chứng giả thuyết trên, nhóm học sinh tiến hành thí nghiệm ở điều kiện 25°C, áp suất 1 bar như sau:
• Bước 1: Chuẩn bị 5 cốc chứa dung dịch ZnSO4 1M, 5 cốc chứa dung dịch AgNO3 có nồng độ lần lượt là 1,00M; 0,50M; 0,10M; 0,05M; 0,01M; các thanh điện cực Zn và Ag có kích thước như nhau; cầu muối; điện kế để đo sức điện động.
• Bước 2: Tiến hành lắp các dụng cụ theo sơ đồ như hình vẽ sau:
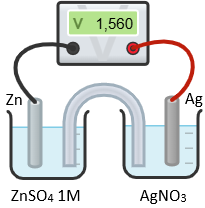
• Bước 3: Lần lượt thay các cốc chứa dung dịch AgNO3 có nồng độ khác nhau, tiến hành đo sức điện động của pin. Kết quả thí nghiệm được học sinh ghi theo bảng sau:
CM AgNO3 (M)…. 1,00….. 0,50….. 0,10….. 0,05….. 0,01
Epin (V)………… 1,560… 1,542… 1,501… 1,483… 1,442
a) Dựa vào kết quả thí nghiệm và lí thuyết điện hoá, giả thiết của học sinh đưa ra là hợp lý.
b) Chiều dòng điện di chuyển từ thanh Zn sang thanh Ag.
c) Khi nồng độ dung dịch AgNO3 là 0,10 M thì sức điện động chuẩn của pin là 1,501 V.
d) Từ kết quả thí nghiệm, tính được thế điện cực chuẩn của Ag+/Ag (khi nồng độ Ag+ bằng 0,50M) là 0,872V biết E°Zn2+/Zn = -0,76V.
Câu trả lời tốt nhất
(a) Sai.
Phản ứng trong pin: Zn(s) + 2Ag+(aq) —> Zn2+(aq) + 2Ag(s)
Biểu thức Nernst:
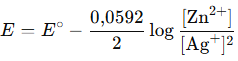
—> [Ag+] giảm thì E giảm, nhưng [Zn2+] giảm thì E tăng.
Như vậy giả thiết của nhóm là sai, nó chỉ đúng đối với Ag+ nhưng không đúng đối với Zn2+.
(b) Sai, chiều dòng điện là chiều của hạt mang điện dương, hoặc ngược chiều của hạt mang điện âm. Nếu xét ở mạch ngoài (khi pin hoạt động) sẽ có dòng electron từ Zn tới Ag, tức là chiều dòng điện từ Ag tới Zn.
Với hệ thống như hình vẽ và mặc định là vôn kế có điện trở vô cùng lớn thì coi như mạch ngoài hở, không có dòng electron, đồng nghĩa với không có dòng điện, pin không hoạt động.
(c) Sai, sức điện động chuẩn được đo trong điều kiện chuẩn (Zn2+, Ag+ cùng nồng độ 1M, ở 25°C). Như vậy E = 1,501V không phải là sức điện động chuẩn, vì lúc đó [Ag+] = 0,10M.
(d) Sai
Thay E = 1,542V; [Ag+] = 0,50M; [Zn2+] = 1M vào biểu thức Nernst ở trên tính được E°Zn-Ag = 1,551
E°Zn-Ag = E°Ag+/Ag – E°Zn2+/Zn
—> E°Ag+/Ag = 0,791V

