Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời CuSO4 và NaCl có cùng nồng độ mol bằng hệ điện phân sử dụng các điện cực than chì.
a) Bán phản ứng xảy ra đầu tiên ở cathode là H2O + 2e → H2 + 2OH-.
b) Khi nước bắt đầu điện phân ở 2 điện cực, khí thoát ra ở anode là Cl2 và H2.
c) Dung dịch sau điện phân có pH < 7.
d) Sinh viên đó tiếp tục thực hiện điện phân theo sơ đồ như hình bên.
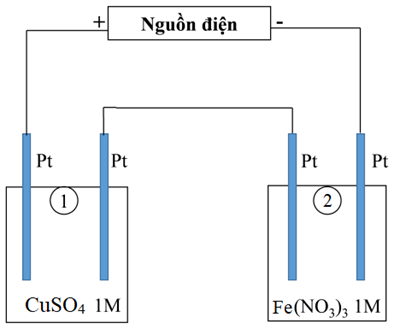
– Bình (1) chứa 200 ml dung dịch CuSO4 1M.
– Bình (2) chứa 300 ml dung dịch Fe(NO3)3 1M. Sau một thời gian, sinh viên quan sát thấy có 5,6 gam kim loại sắt bám lên điệc cực của bình (2). Biết trong hệ điện phân nối tiếp, số điện tử truyền dẫn trong các bình là như nhau. Số gam kim loại Cu bám lên điện cực trong bình (1) là 12,8 gam.
Câu trả lời tốt nhất
(a) Sai, bán phản ứng xảy ra đầu tiên ở cathode là Cu2+ + 2e —> Cu
(b) Sai, khi nước bắt đầu điện phân ở 2 điện cực khí thoát ra là Cl2, O2.
CuSO4 + 2NaCl —> Cu + Cl2 + Na2SO4
CuSO4 + H2O —> Cu + ½O2 + H2SO4
(c) Không rõ, vì không có thông tin về thời điểm kết thúc điện phân.
(d) Đúng
Fe3+ + 1e —> Fe2+
Fe2+ + 2e —> Fe
nFe3+ = 0,3; nFe = 0,1 —> ne = 0,5
nCu2+ = 0,2 < ne/2 —> nCu = 0,2 —> mCu = 12,8 gam

