Nguyên tử nguyên tố X có tổng số hạt electron, proton và neutron là 58. Trong X số hạt mang điện nhiều hơn số hạt không mang điện là 18.
a. Xác định số electron, proton, neutron của X và viết kí hiệu hóa hóa học của X.
b. Nguyên tử X kết hợp với nguyên tử Y tạo thành hợp chất có công thức phân tử X2Y. Trong X2Y có tổng số hạt electron, proton và neutron là 140. Trong X2Y số hạt mang điện chiếm 65,714% tổng số hạt trong X2Y. Xác định công thức hóa học của X2Y.
Câu trả lời tốt nhất
Hạt mang điện: Số electron = Số proton = Z
Hạt không mang điện: Số neutron = N
—> Tổng hạt = 2Z + N = 58
Hạt mang điện nhiều hơn số hạt không mang điện là 18 —> 2Z – N = 18
—> Z = 19; N = 20
—> A = Z + N = 39
Kí hiệu: 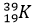
b. Mỗi nguyên tử Y có:
Hạt mang điện: Số electron = Số proton = Z’
Hạt không mang điện: Số neutron = N’
Tổng hạt = 2Z’ + N’ + 58.2 = 140
Số hạt mang điện = 2Z’ + 2.2Z = 65,714%.140
—> Z’ = 8; N’ = 8
—> Y là O, hợp chất là K2O.
