Nhỏ từ từ dung dịch Ba(OH)2 vào dung dịch chứa Al2(SO4)3 và AlCl3, thu được kết tủa có khối lượng m (gam) theo số mol Ba(OH)2 như đồ thị hình bên.
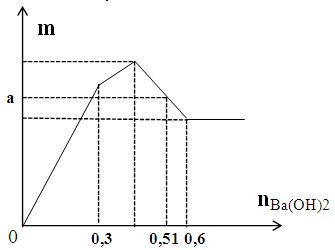
Giá trị của a là:
A. 85,50. B. 163,2. C. 82,38 D. 83,94.
Câu trả lời tốt nhất
Đoạn 1: Tạo ra cả 2 kết tủa
3Ba(OH)2 + Al2(SO4)3 —> 3BaSO4 + 2Al(OH)3
0,3…………………0,1…………..………0,3…………0,2
Đặt nAlCl3 = x
Để tạo ra và hòa tan hết kết tủa Al(OH)3 cần 0,6 mol Ba(OH)2, khi đó nOH- = 4nAl3+
—> 0,6.2 = 4(0,1.2 + x) —> x = 0,1
Khi nBa(OH)2 = 0,51 thì nBaSO4 = 0,3
Lúc này nOH- = 1,02 và nAl3+ tổng = 0,3
nOH- = 4nAl3+ – nAl(OH)3 —> nAl(OH)3 = 0,18
—> a = mBaSO4 + mAl(OH)3 = 83,94 gam
×

