Câu 1. Nhỏ từ từ dung dịch Ba(OH)2 vào ống nghiệm chứa dung dịch HCl và Al2(SO4)3. Đồ thị biểu diễn sự phụ thuộc của khối lượng kết tủa theo thể tích dung dịch Ba(OH)2 như sau:
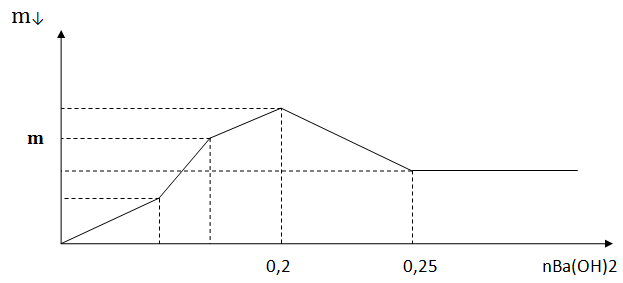
Giá trị của m là:
A. 41,65 B. 40,15 C. 35,32 D. 38,64
Câu 2. Nhỏ từ từ dung dịch Ba(OH)2 vào ống nghiệm chứa dung dịch gồm HCl và Al2(SO4)3. Đồ thị biểu diễn sự phụ thuộc của khối lượng kết tủa ( m gam) theo số mol Ba(OH)2 như sau:
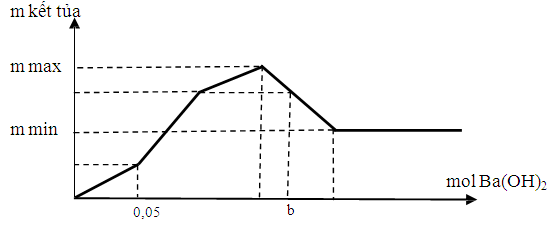
Biết giá trị (mmax – mmin) là 14,04 gam. Hãy cho biết b gần nhất với giá trị nào sau đây ?
A. 0,3. B. 0,2. C. 0,1. D. 0,6.
Câu 3. Nhỏ từ từ dung dịch Ba(OH)2 vào ống nghiệm chứa dung dịch HCl và Al2(SO4)3. Đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa theo số mol Ba(OH)2 được thể hiện như sau:
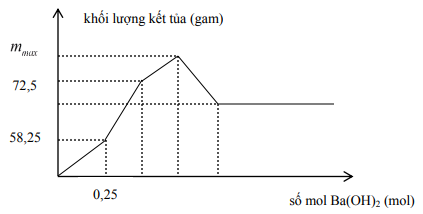
Nếu cho từ từ đến hết 0,6 mol Ba(OH)2 vào ống nghiệm thì khối lượng kết tủa thu được là
A. 85,5 gam. B. 77,7 gam. C. 69,9 gam. D. 82,9 gam.
Câu trả lời tốt nhất
Câu 1.
nHCl = u và nAl2(SO4)3 = v
—> nH+ = u, nAl3+ = 2v và nSO42- = 3v
Trong khi Ba2+ tạo kết tủa ngay từ đầu thì OH- lại phải trung hòa H+ trước rồi mới tạo kết tủa sau. Do đó Ba2+ sẽ kết thúc phản ứng trước OH-.
—> BaSO4 đạt max khi kết thúc đoạn thứ 2 và nBaSO4 max = 3v. Lúc này Al(OH)3 mới tạo ra được một lượng là:
nAl(OH)3 = (6v – u)/3
Khi bắt đầu vào đoạn 3 thì nAl3+ = 2v – (6v – u)/3 = u/3
Để kết tủa nốt lượng Al3+ này cần:
nBa(OH)2 = 0,2 – 3v
Vậy: 2(0,2 – 3v) = 3.u/3 (1)
Khi kết tủa không thay đổi:
nOH- = 0,25.2 = u + 4.2v (2)
(1)(2) —> u = 0,1 và v = 0,05
Kết thúc đoạn 2 lượng kết tủa bao gồm:
nBaSO4 max = 3v = 0,15
nAl(OH)3 = (6v – u)/3 = 1/15
—> m = 40,15
Câu 2.
Đoạn 1:
H+ + OH- —> H2O
Ba2+ + SO42- —> BaSO4
—> nHCl = nOH- = 0,1
Đặt nAl2(SO4)3 = a
Trong khi Ba2+ tạo kết tủa ngay từ đầu thì OH- lại phải trung hòa H+ trước rồi mới tạo kết tủa sau. Do đó Ba2+ sẽ kết thúc phản ứng trước OH-.
—> BaSO4 đạt max khi kết thúc đoạn thứ 2 và Al(OH)3 đạt max khi kết thúc đoạn 3
—> nBaSO4 max = 3a và nAl(OH)2 max = 2a
—> m max – m min = mAl(OH)3 = 78.2a = 14,04
—> a = 0,09
Khi kết thúc đoạn 2 thì kết tủa gồm BaSO4 (3a) —> nOH- = 6a
—> nAl(OH)3 = (6a – 0,1)/3 = 11/75
Tại điểm đang xét (Ứng với b mol Ba(OH)2) thì lượng kết tủa giống điểm kết thúc đoạn 2 nên:
nOH- = nH+ + 4nAl3+ – nAl(OH)3 = 0,1 + 4.2a – 11/75 = 101/150
—> b = nOH-/2 = 101/300 = 0,3367
Câu 3.
Đoạn 1:
H+ + OH- —> H2O
Ba2+ + SO42- —> BaSO4
—> nH+ = nOH- = 0,5
Đoạn 2:
Al3+ + 3OH- —> Al(OH)3
Ba2+ + SO42- —> BaSO4
nBaSO4 = a —> nOH- = 2a = 0,5 + 3nAl(OH)3
—> nAl(OH)3 = (2a – 0,5)/3
—> m↓ = 233a + 78(2a – 0,5)/3 = 72,5
—> a = 0,3
Vậy dung dịch ban đầu chứa HCl (0,5) và Al2(SO4)3 (0,1). Khi thêm 0,6 mol Ba(OH)2:
nBa2+ = 0,6 và nSO42- = 0,3 —> nBaSO4 = 0,3
nOH- = 1,2 và nH+ = 0,5, nAl3+ = 0,2 —> nAl(OH)3 = 0,1
—> m↓ = 77,7 gam

