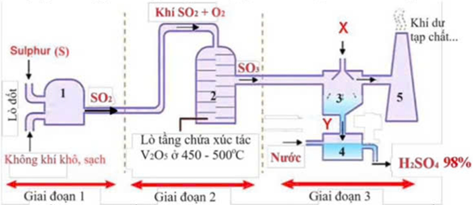
Sulfuric acid (H2SO4) là hợp chất quan trọng trong công nghiệp hoá chất, được sử dụng nhiều trong sản xuất phân bón, khai khoáng, chế biến dầu mỏ,…Trong công nghiệp, sulfuric acid 98% được sản xuất từ sulfur theo quy trình tiếp xúc, sử dụng thiết bị phản ứng dòng liên tục, mô tả trong hình dưới đây:
Câu 1. Cho các phát biểu sau:
(a) Số oxi hoá của sulfur thay đổi qua các giai đoạn: giai đoạn 1 từ 0 lên +4, giai đoạn 2 từ +4 lên +6.
(b) Trong giai đoạn 3, hoá chất X được thêm vào thiết bị phản ứng số 3 và thu được sản phẩm Y. X và Y lần lượt là oleum, H2SO4 đặc.
(c) Trong giai đoạn 2: 2SO2(g) + O2(g) ⇋ 2SO3(g); chất xúc tác V2O5, nhiệt độ khoảng 450°C, để tăng hiệu suất của phản ứng tạo thành SO3 thì cần giảm áp suất của phản ứng.
(d) Khí thải có chứa SO2 nếu không được xử lý thải ra môi trường sẽ góp phần gây ra hiện tượng phú dưỡng.
(đ) Để xác định công thức của Y, người ta pha loãng 8,36 gam Y vào nước thành 1,0 lít dung dịch Z, sau đó tiến hành chuẩn độ mỗi 10,0 mL dung dịch Z này bằng dung dịch NaOH 0,10M. Thể tích NaOH trung bình cần sử dụng để chuẩn độ là 20,0 mL, người ta đã xác định được trong phân tử Y có tổng 23 nguyên tử.
Số phát biểu đúng là
A. 4. B. 2. C. 1. D. 3.
Câu 2.
a) Chất xúc tác ở giai đoạn 2 làm tăng tốc độ phản ứng và tăng hiệu suất tổng hợp SO3.
b) Mục đích dùng lượng dư không khí để phản ứng xảy ra hoàn toàn.
c) X là H2SO4 đặc, Y là H2SO4.nSO3 (oleum).
d) Theo tiêu chuẩn quốc tế quy định nếu lượng SO2 vượt quá 1,0.10-5 mol/m³ không khí thì bị coi là ô nhiễm. Kết quả phân tích 50 lít không khí có 0,042 mg SO2, vì vậy không khí bị ô nhiễm.
Câu trả lời tốt nhất
Câu 1.
(a) Đúng, giai đoạn 1 từ 0 lên +4 (S + O2 —> SO2), giai đoạn 2 từ +4 lên +6 (2SO2 + O2 ⇋ 2SO3).
(b) Sai, X là H2SO4 đặc, Y là oleum.
(c) Sai, chiều thuận có số phân tử khí giảm nên để tăng hiệu suất của phản ứng tạo thành SO3 thì cần tăng áp suất của phản ứng.
(d) Sai, khí SO2 nếu không được xử lý sẽ gây ra hiện tượng mưa acid.
(đ) Đúng
nNaOH = 2 mmol —> nNa2SO4 = 1 mmol
Bảo toàn S —> nH2SO4.nSO3 (ứng với 0,0836 gam hay 83,6 mg) = 1/(n + 1)
M oleum = 98 + 80n = 83,6(n + 1)
—> n = 4: Oleum Y là H2SO4.4SO3 (Tổng 23 nguyên tử)
Câu 2.
(a) Sai, chất xúc tác làm tăng tốc độ phản ứng (cả thuận và nghịch), giúp hệ nhanh đạt trạng thái cân bằng nhưng không làm tăng hiệu suất.
(b) Sai, phản ứng thuận nghịch 2SO2 + O2 ⇋ 2SO3 không thể xảy ra hoàn toàn cho dù có dùng không khí dư. Không khí dư giúp cân bằng này chuyển dịch theo chiều thuận nhiều hơn.
(c) Đúng
(d) Đúng
nSO2 = 0,042.10^-3/64 = 6,5625.10^-7 mol
V = 50 L = 0,05 m³
—> Nồng độ = nSO2/V = 1,3125.10^-5 vượt quá mức 1,0.10^–5 mol/m³ nên không khí bị ô nhiễm.

