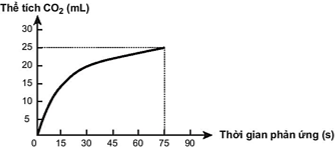
Thực hiện phản ứng sau: CaCO3 + 2HCl → CaCl2 + CO2 + H2O. Theo dõi và ghi lại thể tích khí CO2 thoát ra theo thời gian, thu được đồ thị như sau (Thể tích khí đo được ở áp suất khí quyển và nhiệt độ phòng).
Câu 1. Trong các phát biểu sau, phát biểu nào không đúng?
A. Ở thời điểm 90 giây, tốc độ phản ứng bằng 0.
B. Khi phản ứng hóa học xảy ta, tốc độ phản ứng giảm dần theo thời gian.
C. Tốc độ trung bình của phản ứng trong khoảng thời gian từ thời điểm đầu đến 75 giây là 0,33 mL/s.
D. Tốc độ trung bình của phản ứng trong các khoảng thời gian 15 giây là như nhau.
Câu 2.
a. Nhìn đồ thị cho biết tốc độ phản ứng biến đổi như thế nào theo thời gian?
b. Tính tốc độ trung bình của phản ứng (mL/s) trong khoảng thời gian từ ban đầu đến 75 giây.
c. Thời gian cần để hoà tan hết một mẫu CaCO3 trong dung dịch HCl được biểu diễn ở bảng sau:
Nhiệt độ (°C)………20……….40……..55
Thời gian (phút)……27………..3……….t
Tính giá trị t.
Câu trả lời tốt nhất
Câu 1.
A. Đúng, lúc 90s phản ứng đã kết thúc do ít nhất một trong các chất tham gia phản ứng đã hết.
B. Đúng, lượng CO2 thoát ra chậm dần nên tốc độ phản ứng giảm dần theo thời gian.
C. Đúng, sau 75s thu được 25 mL khí CO2 nên tốc độ trung bình là 25/75 = 0,33 mL/s.
D. Sai, tốc độ trung bình trong 15s sau sẽ thấp hơn tốc độ trung bình trong 15s ngay trước đó.
Câu 2.
(a) Tốc độ thoát khí CO2 chậm dần nên tốc độ phản ứng chậm dần theo thời gian.
(b) v trung bình = 25/75 = 0,33 mL/s.
(c) Theo bảng thì khi nhiệt độ tăng 20°C (từ 20 lên 40) thì tốc độ phản ứng tăng lên 9 lần.
—> λ^(20/10) = 9 —> λ = 3
Khi nhiệt độ tăng 35°C (từ 20 lên 55) thì tốc độ phản ứng tăng lên 3^(35/10) = 46,765 lần
—> t = 27/46,765 = 0,577 phút
