Tiến hành thí nghiệm theo các bước sau:
• Bước 1. Cho vào cốc thủy tinh 30 mL dung dịch H2SO4 0,5 M.
• Bước 2. Cho một lá nhôm và một lá đồng vào cốc sao cho chúng không tiếp xúc với nhau. Để yên khoảng 1 phút.
• Bước 3. Dùng dây dẫn điện nối lá nhôm với lá đồng với một vôn kế (như hình vẽ).
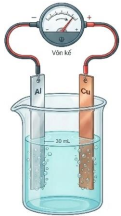
Biết: E°Al3+/Al = -1,676V; E°2H+/H2 = 0,0V; E°Cu2+/Cu = +0,340V .
a) Ở bước 3, kim vôn kế chỉ 1,336 V.
b) Ở bước 3, khí chỉ thoát ra ở bề mặt lá đồng, còn lá nhôm không có khí thoát ra.
c) Ở bước 2, lá nhôm bị ăn mòn hóa học còn lá đồng không bị ăn mòn.
d) Ở bước 3, có sự tạo thành cặp pin điện hóa, trong đó lá nhôm là cathode và lá đồng là anode.
Câu trả lời tốt nhất
(a) Sai, dung dịch chứa H+ 1M, không chứa Cu2+ nên điện cực Cu chỉ là vật dẫn điện. Lúc này:
E° = E°2H+/H2 – E°Al3+/Al = 1,676V
Chú ý: Ban đầu chưa có sẵn Al3+ nên kim điện kế có thể vọt lên một chút sau đó nhanh chóng quay về gần 1,676V.
(b) Sai, khí H2 chủ yếu thoát ra trên bề mặt điện cực Cu (do ăn mòn điện hóa của cặp Al-Cu), nhưng bản thân Al vẫn bị ăn mòn hóa học nên vẫn có một lượng nhỏ bọt khí thoát ra bên cực Al.
(c) Đúng, Al bị ăn mòn nhanh chóng do phản ứng trực tiếp với H2SO4. Trong thời gian ngắn của thí nghiệm thì không thấy Cu bị ăn mòn do Cu không phản ứng với H2SO4 loãng (nếu để lâu thì Cu vẫn bị ăn mòn, với hỗ trợ từ O2 trong không khí hòa tan trong dung dịch).
(d) Sai, Al là anode, Cu là cathode.

