Trong một bình kín có thể tích 1 lít chứa 0,5 mol H2 và 0,3 mol I2. Nung nóng bình đến nhiệt độ 430°C khi đó xảy ra phản ứng: H2(g) + I2(g) ⇋ 2HI(g) Kc = 54.
Giữ nguyên nhiệt độ đó đến khi phản ứng đạt đến trạng thái cân bằng một thời gian. Hãy
+ Tính nồng độ mol/L của các chất khi đạt đến trạng thái cân bằng và vẽ dạng đồ thị biểu diễn sự biến đổi nồng độ mol/L của các chất trong bình theo thời gian phản ứng trong quá trình trên.
+ Sau khi phản ứng đạt đến trạng thái cân bằng ở nhiệt độ 430°C, nếu giảm thể tích bình thì nồng độ mol/L của các chất trong bình có thay đổi không? Giải thích.
Câu trả lời tốt nhất
H2(g) + I2(g) ⇋ 2HI(g)
0,5………0,3………0
x………….x………..2x
0,5-x……0,3-x…….2x
Kc = (2x)²/(0,5 – x)(0,3 – x) = 54
—> x = 0,27508
Ở trạng thái cân bằng:
[H2] = 0,5 – x = 0,22492
[I2] = 0,3 – x = 0,02492
[HI] = 2x = 0,55016
Dạng đồ thị:
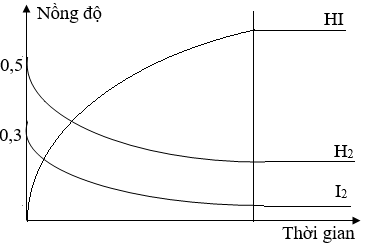
Số phân tử khí của 2 vế như nhau nên giảm thể tích không làm cho cân bằng chuyển dịch, số mol các khí không thay đổi nhưng thể tích giảm nên nồng độ các khí đều tăng.

