Xăng sinh học E5 là nhiên liệu chứa 5% thể tích ethanol và 95% thể tích xăng truyền thống. Sử dụng xăng sinh học được coi là giải pháp bảo vệ môi trường, giảm sự phụ thuộc vào nhiên liệu hóa thạch. Coi thể tích xăng E5 bằng tổng thể tích xăng truyền thống (D = 0,700 g/cm³) và C2H5OH (D = 0,789 g/cm³). Biết xăng truyền thống là hỗn hợp của C8H18 và C9H20 (tỷ lệ mol tương ứng là 5 : 4). Ở cùng điều kiện phản ứng, đốt cháy hoàn toàn:
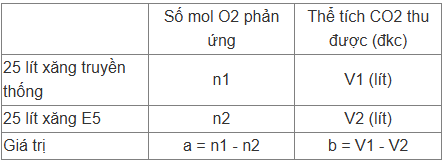
Giá trị của a và b gần nhất là
A. 32,4 và 470,8. B. 31,5 và 470,8.
C. 32,4 và 460,6. D. 31,5 và 460,6.
Câu trả lời tốt nhất
C8H18 + 12,5O2 —> 8CO2 + 9H2O
C9H20 + 14O2 —> 9CO2 + 10H2O
C2H5OH + 3O2 —> 2CO2 + 3H2O
• Đốt 25 L xăng truyền thống:
nC8H18 = 5x; nC9H20 = 4x
—> 114.5x + 128.4x = 25000.0,7
—> x = 16,17375
n1 = 12,5.5x + 14.4x = 1916,58938 mol
V1 = 24,79(8.5x + 9.4x) = 30471,9920 L
• Đốt 25 L xăng E5:
nC2H5OH = 25000.5%.0,789/46 = 21,44022 mol
nC8H18 = 5y; nC9H20 = 4y
—> 114.5y + 128.4y = 25000.95%.0,7
—> y = 15,36506
n2 = 12,5.5y + 14.4y + 21,44022.3 = 1885,08027 mol
V2 = 24,79(8.5y + 9.4y + 21,44022.2) = 30011,39375 L
a = n1 – n2 = 31,5
b = V1 – V2 = 460,6

