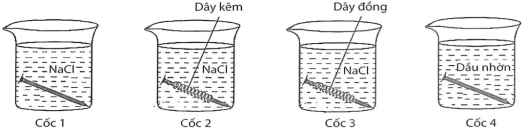
Tiến hành thí nghiệm (như hình vẽ): Rót dung dịch NaCl bão hoà vào cốc 1, cốc 2, cốc 3; cho dầu nhờn vào cốc 4. Cho vào cốc 1 và cốc 4 một đinh sắt sạch, cho vào cốc 2 đinh sắt sạch được quấn bởi dây kẽm, cho vào cốc 3 đinh sắt sạch được quấn bởi dây đồng. Để 4 cốc trong không khí khoảng 5 ngày.
a) Ở cốc 4, đinh sắt không bị gỉ. Do đó các đồ vật bằng sắt có thể bảo vệ bằng cách tra dầu mỡ.
b) Để bảo vệ tàu biển làm bằng thép, người ta gắn các tấm kẽm lên vỏ tàu (phần chìm dưới nước).
c) Ở cốc 1, đinh sắt bị gỉ và dung dịch có màu vàng của FeCl2. Ở cốc 2, đinh sắt không bị gỉ, dây Zn bị ăn mòn.
d) Ở cốc 3, đinh sắt bị gỉ nhiều nhất và dây đồng không bị ăn mòn.
Câu 2. Có các nhãn chú thích sau:
(a) Thí nghiệm minh họa, bảo vệ kim loại khỏi ăn mòn bằng phương pháp phủ bề mặt
(b) Thí nghiệm minh họa, bảo vệ kim loại khỏi ăn mòn bằng phương pháp điện hóa
(c) Thí nghiệm minh họa ăn mòn điện hóa dây dẫn hai kim loại khác nhau
Thứ tự các cốc tương ứng lần lượt với các nhãn a, b, c là? (lưu ý giả sử thứ tự đúng là cốc 1, 2, 3 ứng với các nhãn a, b, c thì sẽ ghi đáp án là 123)
Câu 3. Trong thí nghiệm trên, ở cốc nào đinh sắt được bảo vệ bằng phương pháp phủ bề mặt?
A. Cốc 2. B. Cốc 3. C. Cốc 4. D. Cốc 1.
Câu 4. Ở cốc 2 và cốc 3, hiện tượng và cách giải thích nào sau đây đúng?
A. Cả hai cốc đều xảy ra sự ăn mòn hóa học do kim loại tiếp xúc trực tiếp với dung dịch chất điện li NaCl.
B. Ở cốc 2, zinc bị ăn mòn; ở cốc 3, sắt là cực âm của pin điện hóa nên bị ăn mòn.
C. Ở cốc 2, zinc đóng vai trò là cực dương nên sắt bị ăn mòn; ở cốc 3, copper đóng vai trò cực âm nên sắt được bảo vệ.
D. Ở cốc 2, sắt bị ăn mòn điện hóa; ở cốc 3, sắt không bị ăn mòn do copper đã nhận hết electron.
Câu trả lời tốt nhất
Câu 1.
(a) Đúng, dầu nhờn tạo môi trường không điện li và ngăn O2 tiếp xúc với đinh sắt nên đinh sắt không bị ăn mòn.
(b) Đúng, Zn có tính khử mạnh hơn sắt nên Zn sẽ bị ăn mòn và sắt được bảo vệ.
(c) Sai, ở cốc 1 đinh sắt có lớp gỉ màu nâu đỏ của Fe(OH)3, ở cốc 2, đinh sắt không bị gỉ, dây Zn bị ăn mòn:
2Fe + O2 + 2H2O —> 2Fe(OH)2
4Fe(OH)2 + O2 + 2H2O —> 4Fe(OH)3
(d) Đúng, ở cốc 3 Fe có tính khử mạnh hơn Cu nên đinh sắt bị ăn mòn và dây đồng không bị ăn mòn. Ở cốc 3 sắt bị ăn mòn điện hóa nên tốc độ ăn mòn nhanh hơn ăn mòn hóa học ở cốc 1.
Câu 2.
(a) Cốc 4 là thí nghiệm minh họa bảo vệ kim loại khỏi ăn mòn bằng phương pháp phủ bề mặt: dầu nhờn không điện ly, tạo lớp ngăn cách kim loại với môi trường xung quanh.
(b) Cốc 2 là thí nghiệm minh họa bảo vệ kim loại khỏi ăn mòn bằng phương pháp điện hóa trong đó kim loại Zn có tính khử mạnh hơn đóng vai trò là anode và bị oxi hóa, đinh sắt là cathode được bảo vệ.
(c) Cốc 3 là thí nghiệm minh họa ăn mòn điện hóa dây dẫn hai kim loại khác nhau trong đó đinh sắt là anode và bị oxi hóa.
Chú ý: Cốc 2 và 3 đều có ăn mòn điện hóa nhưng chủ thể ta đang xét để đối chiếu và so sánh với cốc 1 và cốc 4 là đinh sắt, vì vậy đối tượng quan sát là đinh sắt.
Câu 3.
Đinh sắt được bảo vệ bằng phương pháp phủ bề mặt ở cốc 4: Dầu nhờn tạo lớp ngăn cách đinh sắt với môi trường, không cho phép hơi nước và không khí thấm qua.
Câu 4.
A. Sai, cả 2 cốc đều xảy ra ăn mòn điện hóa do các kim loại tiếp xúc trực tiếp với nhau (Zn-Fe, Fe-Cu), đồng thời tiếp xúc trực tiếp với dung dịch điện li NaCl có hòa tan O2 từ không khí.
B. Đúng, kim loại có tính khử mạnh hơn là cực âm và bị ăn mòn (Zn ở cốc 2 và Fe ở cốc 3).
C. Sai, ở cốc 2 thì Zn là cực âm nên Zn bị ăn mòn, Fe được bảo vệ. Ở cốc 3 thì Fe là cực âm nên Fe bị ăn mòn, Cu được bảo vệ.
D. Sai, ở cốc 2, Zn bị ăn mòn điện hóa. Ở cốc 3 Cu nhận electron nên Fe mới bị ăn mòn.
dạ cho em hỏi, ở cốc số 2, có bọt khí thoát ra không, giải thích tại sao ạ
dạ với cho em hỏi thêm là nếu ở cốc số 3 thay dung dịch nacl bằng nước cất thì đinh có bị gỉ không và tại sao lại vậy ạ?
cho e hỏi cốc số 1 có sự ăn mòn điện hóa là đúng hay sai ạ
