Trong công nghiệp, quá trình điện phân dung dịch NaCl thường được tiến hành trong thùng điện phân có anode bằng than chì và cathode bằng sắt (giữa hai điện cực có màng ngăn xốp) dùng để sản xuất NaOH, khí Cl2. Sơ đồ quá trình điện phân dung dịch NaCl trong công nghiệp như hình vẽ sau:
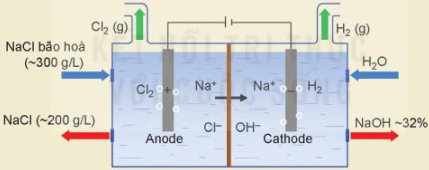
Dung dịch NaCl bão hòa có nồng độ 300 g/L bơm vào chỉ được điện phân một phần thành dung dịch NaCl có nồng độ 200 g/L, dung dịch này sau đó được dẫn ra khỏi thùng điện phân, trong khi nước muối mới được bơm vào. Việc làm này giúp hạn chế sự tạo thành sản phẩm không mong muốn. Dung dịch NaOH thu được ở cathode có nồng độ 32% được chuyển sang thiết bị cô đặc để sản xuất dung dịch NaOH có nồng độ theo ý muốn.
a) Tại cathode xảy ra sự khử H2O thành khí H2 và OH-, tại anode xảy ra sự oxi hóa ion Cl- thành khí Cl2.
b) Giả sử NaOH không bị thất thoát trong quá trình cô đặc, thể tích dung dịch NaCl không thay đổi trong quá trình điện phân. Để sản xuất được một thùng 20 lít dung dịch NaOH 40% thương phẩm có khối lượng riêng 1,5 g/mL, cần ít nhất 175,5 lít dung dịch NaCl bão hòa nồng độ 300 g/L bơm vào thùng điện phân.
c) Khí Cl2 thoát ra ở cathode, khí H2 thoát ra ở anode.
d) Màng ngăn xốp có tác dụng ngăn không cho khí Cl2 chuyển sang cathode phản ứng với OH-.
Câu trả lời tốt nhất
(a) Đúng:
Cathode: 2H2O + 2e —> H2 + 2OH-
Anode: 2Cl- —> Cl2 + 2e
(b) Đúng
mNaOH = 20.1,5.40% = 12 kg
—> mNaCl phản ứng = 12.58,5/40 = 17,55
Dung dịch NaCl đi vào (0,3 kg/L) và dung dịch NaCl đi ra (0,2 kg/L)
—> V = 17,55/(0,3 – 0,2) = 175,5 L
(c) Sai, khí H2 thoát ra ở cathode, khí Cl2 thoát ra ở anode
(d) Đúng

