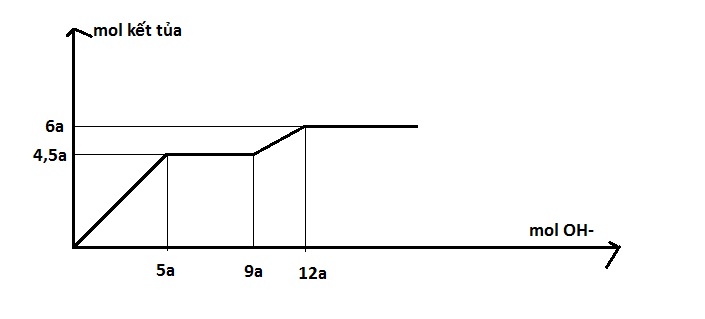
Hỗn hợp X chứa Na, Na2O, Na2CO3, ZnCO3 (trong đó oxi chiếm 28,905% về khối lượng hỗn hợp). Hòa tan hết 18,82 gam X vào dung dịch chứa HCl 0,5M và H2SO4 0,6M. Sau khi kết thúc phản ứng thu được dung dịch Y và hỗn hợp khí Z có tỉ khối so với He bằng 5,75. Cho dung dịch Ba(OH)2 dư vào Y, phản ứng được biểu diễn theo đồ thị:
Phần trăm khối lượng Na2O trong X là:
A. 13,2% B. 19,8% C. 9,9% D. 3,3%
Câu trả lời tốt nhất
Khi nOH- = 12a —> nBa(OH)2 = 6a thì kết tủa không thay đổi nữa, lúc này chỉ còn BaSO4.
—> nH2SO4 ban đầu = nBaSO4 = 6a
—> nHCl = 5a
Khi nOH- = 5a —> nBa(OH)2 = 2,5a
—> nBaSO4 = 2,5a và nZn(OH)2 = 4,5a – 2,5a = 2a
nOH- = nH+ + 2nZn(OH)2 —> nH+ dư = a
Khi nOH- = 9a —> nBa(OH)2 = 4,5a
—> nBaSO4 = 4,5a —> nZn(OH)2 = 0
—> OH- đoạn 2 hòa tan Zn(OH)2 tạo ra ở đoạn 1 nên đoạn 1 đã tạo Zn(OH)2 max.
—> nZn2+ = nZn(OH)2 = 2a
Đoạn 3 thì OH- không tham gia phản ứng nào, chỉ có Ba2+ kết tủa hết lượng SO42- còn lại.
Khi kết thúc đoạn 3 thì phần dung dịch chứa ZnO22- (2a), Cl- (5a), OH- (3a), bảo toàn điện tích —> nNa+ = 12a
Dung dịch Y chứa Na+ (12a), Zn2+ (2a), H+ (a), Cl- (5a), SO42- (6a)
Quy đổi X thành Na (12a), Zn (2a), O (b) và CO2 (c)
mX = 23.12a + 65.2a + 16b + 44c = 18,82
nO = b + 2c = 18,82.28,905%/16
Bảo toàn electron —> nH2 = 8a – b
mZ = 2(8a – b) + 44c = 5,75.4(8a – b + c)
—> a = 0,03; b = 0,14; c = 0,1
Bảo toàn C —> nNa2CO3 = c – 2a = 0,04
—> nNa2O = b – nNa2CO3 – 2a = 0,04
—> %Na2O = 13,18%
