Cho bảng số liệu sau:
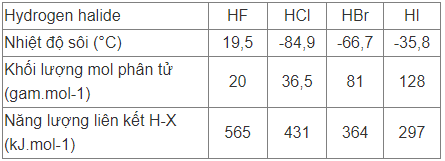
1. Nhận xét và giải thích chiều hướng biến đổi năng lượng liên kết từ HF đến HI. Từ đó so sánh độ bền nhiệt của các HX.
2. Tại sao HF lại có nhiệt độ sôi cao hơn hẳn so với các halogen halide khác? Tại sao từ HCI đến HI nhiệt độ sôi lại tăng?
3. Biểu diễn liên kết hydrogen có thể có trong dung dịch HF.
Câu 2. Phát biểu nào sau đây không đúng?
A. Chiều tăng dần tính acid HF < HCl < HBr < HI.
B. Ở điều kiện thường (25°C), các chất HF, HCl, HBr, HI đều ở thể khí.
C. Nhiệt độ sôi của HF cao bất thường so với các chất còn lại là do năng lượng liên kết H-F lớn.
D. Nhiệt độ sôi HCl < HBr < HI là do tương tác van der Waals giữa các phân tử tăng dần.
Câu trả lời tốt nhất
1. Từ HF đến HI, năng lượng liên kết giảm dần do từ F đến I bán kính nguyên tử tăng ⇒ Bán kính nguyên tử tăng và mật độ điện tích âm trên anion giảm ⇒ Độ dài liên kết tăng ⇒ Năng lượng liên kết giảm.
2. HF có nhiệt độ sôi cao hơn hẳn các HX còn lại vì giữa các phân tử HF có liên kết H liên phân tử, các HX còn lại không có liên kết H liên phân tử.
Từ HCl đến HI phân tử khối các chất tăng ⇒ Tương tác Vander walls tăng ⇒ Nhiệt độ sôi tăng.
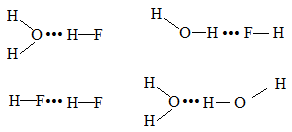
3. Các liên kết H trong dung dịch HF:
Câu 2.
A. Đúng, bán kính X- tăng dần nên mật độ điện âm trên X- giảm dần, lực hút với H+ cũng giảm dần. Mặt khác, độ dài liên kết tăng cũng làm lực hút với H+ cũng giảm, kết quả là tính acic tăng HF < HCl < HBr < HI.
B. Đúng, nhiệt độ sôi các HX đều nhỏ hơn 25°C nên tại 25°C các chất HF, HCl, HBr, HI đều ở thể khí.
C. Sai, HF có nhiệt độ sôi cao hơn hẳn các HX còn lại vì giữa các phân tử HF có liên kết H liên phân tử, các HX còn lại không có liên kết H liên phân tử.
D. Đúng, phân tử càng lớn, tương tác van der Waals càng mạnh.

