Cho từ từ từng giọt dung dịch Ba(OH)2 loãng đến dư vào dung dịch chứa a mol Al2(SO4)3 và b mol Na2SO4. Khối lượng kết tủa (m gam) thu được phụ thuộc vào số mol Ba(OH)2 (n mol) được biểu diễn bằng đồ thị như hình sau:
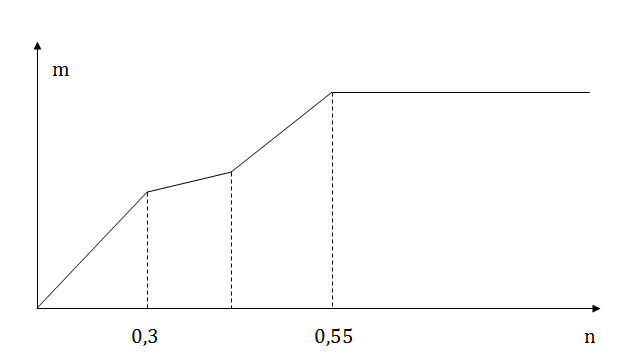
Giá trị tỉ lệ a : b tương ứng là
A. 1:1. B. 2:3. C. 1:2. D. 2:5.
Câu trả lời tốt nhất
Đoạn 1:
3Ba(OH)2 + Al2(SO4)3 —> 3BaSO4 + 2Al(OH)3
0,3…………………0,1………………………….0,2
—> a = 0,1
Khi kết tủa không thay đổi thì dung dịch chứa Na+ (2b), AlO2- (0,2), bảo toàn điện tích —> OH- dư (2b – 0,2)
nOH- = 4nAl3+ + nOH- dư
⇔ nOH- = 0,55.2 = 0,1.2.4 + (2b – 0,2)
—> b = 0,25
—> a : b = 2 : 5
Chú ý:
Đoạn 2: Hòa tan hết Al(OH)3
Al(OH)3 + OH- —> AlO2- + H2O
Ba2+ + SO42- —> BaSO4
Đoạn 3: Kết tủa hết phần SO42- còn lại
Ba2+ + SO42- —> BaSO4
